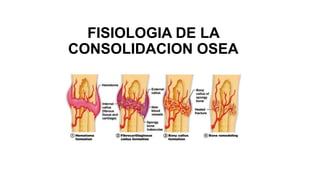
Fisiología consolidación fracturas ósea
- 1. FISIOLOGIA DE LA CONSOLIDACION OSEA
- 2. INTRODUCCIÓN • La curación de fracturas implica un conjunto complejo y secuencial de eventos para restaurar el hueso. • Las células madre son cruciales para el proceso de reparación de fracturas. • El periostio y el endostio son las dos fuentes principales. • La estabilidad de la fractura dicta el tipo de curación que ocurrirá.
- 5. CONSOLIDACIÓN ÓSEA PRIMARIA, DIRECTA O CORTICAL • Se produce mediante remodelación de hueso cortical directa en el foco de fractura. • Curación intramembranosa (Remodelación haversiana) • NO SE PRODUCE CALLO ÓSEO. • CONDICIONES: α Fracturas perfectamente reducidas, con una adecuada compresión entre ellos y estabilidad absoluta del foco de fractura. α Estas condiciones son las más difíciles de obtener, por lo que este tipo de consolidación es poco frecuente.
- 6. CONSOLIDACIÓN ÓSEA INDIRECTA O SECUNDARIA • Se produce mediante la FORMACIÓN DE CALLO ÓSEO. • Curación endocondral. • Implica respuestas en el periostio y los tejidos blandos externos. • Fracturas que presentan un espacio entre los fragmentos óseos, baja compresión y/o inestabilidad en el foco de fractura. • Ocurre con fijación no rígida, como aparatos ortopédicos para fracturas, fijación externa, placas de puente, clavos intramedulares.
- 7. Etapas de la consolidación de fracturas
- 8. INFLAMACIÓN • El hematoma proporciona células hematopoyéticas que producen la liberación de citoquinas que inician una respuesta inflamatoria. • Esta respuesta produce vasodilatación, hiperemia, así como migración y proliferación de neutrófilos, polimorfonucleares y macrófagos. • El hematoma es reemplazado por tejido de granulación y los osteoclastos comienzan a remover el tejido necrótico. • Células mesenquimáticas y fibroblastos proliferan gracias a la expresión de proteínas de la familia TGF-β incluyendo las proteínas morfogenéticas óseas (BMPs). Hematoma de fractura y respuesta inflamatoria Tiempo: 1-7 días PDGF, TNF-Alfa, TGF-Beta, IL-1,6, 10,12 Proliferan osteoblastos y fibroblastos Formación de neovasos
- 9. Descripción general de los factores de crecimiento • Factor • Fuente • Mecanismo • Función TGF-B • Plaquetas, MEC de hueso, matriz de cartílago • Osteoinductivo • El factor de crecimiento pleiotrópico estimula la proliferación de células mensenquimales indiferenciadas • Estimula la producción de colágeno tipo II y proteoglicanos por parte de las células mesenquimales. • Induce a los osteoblastos a sintetizar colágeno. BMP • Pertenecen a la superfamilia TGF-B • Células osteoprogenitoras, osteoblastos, MEC ósea • Osteoinductivo • Promueve la diferenciación de las células mesenquimales en condrocitos y osteoblastos. • Promueve la diferenciación de osteoprogenitores en osteoblastos, influye en la formación del patrón esquelético. • FGF • Macrófagos, células mesenquimales, condrocitos, osteoblastos • Tirosina quinasa • Mitógeno para células mesenquimales, condrocitos y osteoblastos. • IGF • Matriz ósea, osteoblastos, condrocitos • Tirosina quinasa • Promueve la proliferación y diferenciación de células osteoprogenitoras. • PDGF • plaquetas, osteoblastos Quimiotaxis • mitógeno para células mesenquimales y osteoblastos; quimiotaxis de macrófagos.
- 10. REPARARACIÓN • El hematoma de fractura produce una matriz cartilaginosa y una red de nuevos vasos sanguíneos que atrae células progenitoras y factores de crecimiento para la diferenciación de las células mesenquimáticas a osteoblastos. • Este proceso se lleva a cabo a través de la interacción entre BMPs, TGF-β, IGFs. • La inflamación comienza a disminuir y se inicia el proceso de formación de nuevo tejido óseo en la forma de un callo óseo, inicialmente blando y luego duro. • Ambos callos inician su formación de forma paralela, sin embargo el callo duro demora más tiempo en su formación. • La estabilidad otorgada por la formación del callo óseo es axial inicialmente (previene el acortamiento) y de forma más tardía es angular. Formación de callo blando y callo duro Tiempo: 1a-2a semana en adelante
- 11. • El entorno mecánico impulsa la diferenciación de linajes de células osteoblásticas (entorno estable) o condriocíticas (entorno inestable). • La osificación endocondral convierte el callo blando en callo duro (hueso tejido). • El colágeno tipo II (cartílago) se produce temprano en la curación de la fractura y luego sigue la expresión del colágeno tipo I (hueso). • La cantidad de callo es inversamente proporcional al grado de inmovilización.
- 12. CALLO BLANDO • Ocurre en la periferia de la fractura a las 2-3 semanas de la lesión. • Este callo es secundario a la acción de las células osteoprogenitoras y osteoblastos de la capa interna del periostio y del endostio. CALLO DURO • Corresponde a osificación endocondral • Parte de un molde de cartílago que después se osifica por la acción de los osteoblastos. Se inicia en paralelo con el callo blando, pero demora más tiempo (3-4 meses)
- 13. REMODELACIÓN • Comienza en medio de la fase de reparación y continúa mucho después de la consolidación clínica. • El nuevo hueso reticular es inmaduro y presenta una microestructura irregular el cual es remodelado a través de la función conjunta de osteoblastos y osteoclastos restableciéndose su arquitectura microscópica. • Se forma hueso laminillar maduro, en cuyo proceso también actúan TGF-β, BMPs e IGFs. • En esta etapa también se restablece el canal medular. Ley de Wolff
- 14. FACTORES QUE AFECTAN LA CONSOLIDACIÓN ÓSEA
- 15. FACTORES DE LA FRACTURA DISMINUYEN CONSOLIDACIÓN – Conminución. – Compromiso de partes blandas alrededor de la fractura. – Daño perióstico. – Baja presión parcial de oxígeno local (baja irrigación, mala cobertura de partes blandas) – Excesiva separación entre los fragmentos óseos (en general ≥ 2mm) – Inestabilidad del foco de fractura (inmovilización inadecuada) – Infección (fracturas expuestas) – Fracturas intraarticulares (fibrolisina del líquido articular) – Fracturas asociadas a compromiso de circulación terminal (ej.: escafoides, astrágalo, cabeza femoral y odontoides) AUMENTAN CONSOLIDACION – Rasgo simple. – Conservación de partes blandas e irrigación en el foco de fractura – Conservación del periostio. – Alta presión parcial de oxígeno local – Escasa separación entre los fragmentos óseos. – Estabilidad del foco de fractura (evitando excesiva rigidez, ya que ésta puede disminuir la consolidación) – Fracturas sin exposición ni infección. La irrigación es el factor independiente más significativo para lograr la consolidación ósea
- 16. Factores del paciente DISMINUYEN CONSOLIDACIÓN – Edad – Reposo excesivo / postración – Diabetes – Insuficiencia vascular – Desnutrición proteica – Enfermedades asociadas a alteraciones del metabolismo del calcio AUMENTAN CONSOLIDACION – Esqueleto inmaduro – Ejercicio, carga precoz progresiva – Trauma encefálico (neurotropinas y factores neurotrópicos séricos tendrían efecto osteogénico) Factores asociados a medicamentos / hormonas DISMINUYEN CONSOLIDACIÓN – Corticoides (disminuye la diferenciación a osteoblastos) – Nicotina (disminuye irrigación local) – AINEs – Quinolonas (tóxicas para condrocitos) – Metotrexate AUMENTAN CONSOLIDACION – TH (hormona tiroidea) – PTH (hormona paratiroídea) – GH (hormona del crecimiento) – Calcitonina
- 17. Medidas físicas / eléctricas* DISMINUYEN CONSOLIDACIÓN – Excesiva rigidez del foco de fractura – Excesiva movilidad del foco de fractura – Electricidad con corriente alterna (AC)e AUMENTAN CONSOLIDACION – Micro-movimiento del foco de fractura – Ultrasonido con pulsos de baja intensidad (LIPUS) – Terapia de ondas de choque extracorpóreas (ESWT) – Electricidad con corriente directa (DC) y campos electromagnéticos pulsátiles (PEMFs)
- 18. INJERTOS ÓSEOS
- 19. • Osteoconductoras, • Osteoinductivas y/o • Osteogénicas. Autoinjertos Aloinjertos Matriz ósea desmineralizada (DBM) Sintéticos Proteína morfogenética ósea (BMP) Células madre INDICACIONES • Ayudar en la curación de fracturas, uniones retrasadas o pseudoartrosis. • Ayudar en artrodesis y fusiones espinales. • Reemplazar defectos óseos por trauma o tumor. Un material con propiedades…
- 20. PROPIEDADES
- 21. OSTEOCONDUCTIVO Actúa como un marco estructural para el crecimiento óseo. Proporcionan una superficie y una estructura que facilitan a las células madre y progenitoras osteogénicas su EJEMPLOS Matrices óseas desmineralizadas Sustitutos oseos: sulfato de calcio > fosfato tricálcico > hidroxiapatita unión, migración, proliferación, diferenciación y supervivencia
- 22. OSTEOINDUCTIVO El material contiene factores que estimulan el crecimiento óseo y la inducción de células madre en un linaje formador de hueso. Proteína morfogenética ósea (BMP)
- 23. OSTEOGÉNICO El material proporciona directamente células que producirán hueso, incluidas células madre mesenquimales primitivas, osteoblastos y osteocitos. •Las células madre mesenquimales pueden potencialmente diferenciarse en cualquier línea celular. •Las células osteoprogenitoras se diferencian en osteoblastos y luego en osteocitos. El hueso esponjoso tiene una mayor capacidad que el hueso cortical para formar hueso nuevo debido a su mayor área de superficie. El injerto óseo autólogo (autoinjerto fresco y aspirado de médula ósea) es el único material de injerto óseo que contiene células precursoras mensenquimatosas vivas.
- 24. TIPOS DE AUTOINJERTO •Esponjoso •Menos soporte estructural •Mayor osteoconducción •Incorporación rápida a través de sustitución progresiva •Cortical •Incorporación más lenta debido a la necesidad de remodelar los canales Haversion existentes •Laminillas intersticiales conservadas •Proporciona más soporte estructural. •El 25 % de los injertos masivos sufren fracturas por insuficiencia •Injerto óseo vascularizado •Técnicamente desafiante con unión más rápida y preservación celular •Los ejemplos incluyen: injerto de puntal de peroné libre (arteria peronea), cresta ilíaca libre (arterias ilíacas circunflejas profundas), radio distal utilizado para fx de escafoides (1-2 rama de la arteria superretinacular intercompartimental de la arteria radial)