Toxicocinetica Ambiental.pdf
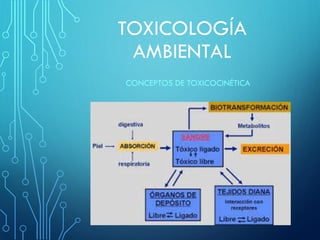
- 2. Es la disciplina que estudia cuantitativamente los procesos de absorción, distribución, biotransformación y eliminación de xenobióticos en el organismo, con el objetivo de calcular su concentración y la evolución de la misma en el tiempo. Toxicocinética
- 3. •La toxicocinética clásica hace uso de modelos compartimentales, en los que distintos órganos o tejidos se agrupan en función de ciertas características. •También hace uso de modelos fisiológicos toxicocinéticos en los que se describen matemáticamente los distintos órganos o tejidos en función de sus características fisiológicas o bioquímicas.
- 4. Diferencias entre ambos modelos •Los MC son una simplificación ideal del organismo basada en una serie de hipótesis restrictivas, tanto fisiológicas como bioquímicas. •Los MFT se formulan sin necesidad de utilizar dichas hipótesis. •Los MFT son de mayor complejidad y parten de consideraciones teóricas y de parámetros medibles experimentalmente. •Los MFT requieren mayor cantidad de datos.
- 5. Consideraciones Cinéticas Cinética: Estudia la evolución en el tiempo de las rxns químicas y, por extensión, del conjunto de procesos físicos, químicos y bioquímicos del que depende la concentración de los compuestos en el organismo y su evolución en el tiempo. Por analogía la toxicocinética estudia la evolución en el tiempo de la concentración de compuestos tóxicos en el organismo, así mismo como resultado de los mencionados procesos.
- 6. Premisia#1 Los procesos de absorción, distribución, biotransformación y eliminación se realizan habitualmente mediante cinética de primer orden. C k dt dC r a a − = = C: conc. Del xenobiótico, ra: velocidad de desaparición, ka: cte de velocidad.
- 7. t k C C e C C dt k C dC a t k a a − = = − = − 0 0 ln ln C0: es la conc. a tiempo cero (la conc. alcanzada al distribuirse homogéneamente el compuesto en plasma inmediatamente después de la administración de la dósis).
- 8. Tiempo de vida media: el tiempo necesario para que las conc. de dicho compuesto descienda hasta alcanzar un valor igual a la mitad de su conc. inicial. a k t 2 ln 2 / 1 = Las expresiones cineticas de 1er orden describen adecuadamente los procesos de abs, distrib, biotransf y elimin para bajas concentraciones de los xenobióticos.
- 9. •A medida que aumenta las conc. de estos, se van prod. desviaciones respecto a la cinética de 1er orden, que obedecen normalmente a procesos de saturación.Ej: complejos con proteínas de la membrana en transportes activos. •Los procesos saturables se representan matem. mediante la ec. de Michaelis-Menten. C K C V dt dC r s a + = = max
- 10. Vmax: velocidad máxima que puede alcanzar la rxn, en exceso del reactivo C; C: conc. del xenobiótico; Ks: cte de MM o cte de semisaturación. C K V dt dC r K K C C K Si V dt dC r C K C K C Si S a S S S a S S max max ; ; = = + = = + Dicha ecuación puede simplificarse en ciertos casos:
- 11. Toxicocinética Clásica: Modelos Compartimentales •Se basan en la división del organismo en bloques o compartimentos homogéneos. •No toman en cuenta consideraciones anatómicas o fisiológicas. •Se fundamenta en la observación experimental, monitoreando la conc. del xenobiótico en el plasma. •Toman en cuenta el flujo sanguíneo en órganos.
- 12. •Constan de al menos un compartimento central que representa el plasma y los tejidos con los que éste alcanza rápidamente el equilibrio, conectado a uno o varios compartimentos periféricos en los que se distribuye el xenobiótico desde el compartimiento central con mayor lentitud. •La eliminación del compuesto engloba los procesos de transformación y excreción
- 14. Modelos Monocompartimentales •Consta de un bloque. •Consideran que la totalidad del organismo se comporta de forma homogénea. •Se aplica a una sola administración de un compuesto. •Se refiere a la concentración del xenobiótico en el plasma. •Supone un equilibrio entre plasma y tejidos.
- 16. La evolución de la [xenobiótico] en el modelo monocompartimental se describe por: t kel e C C − = 0 Kel: cte de 1er orden de eliminación; C0: conc. inicial del compuesto en plasma.
- 17. Modelos Bicompartimentales •Muchos compuestos presentan desviaciones al modelo lineal asumido. •El equilibrio plasma-tejido precisa de mayor tiempo para alcanzarlo. •Requiere de modelos multicompartimentales. •Utiliza un modelo matemático más complejo.
- 19. bt at Be Ae C − − + = Esta curva puede expresarse como: Donde A y B son ctes de proporcionalidad y a y b son las ctes de 1er orden de los procesos de distribución y eliminación, respectivamente. Se observan las fases de distribución y eliminación en este modelo.
- 21. Volumen de distribución aparente = = + + = k j bj bj n i ai ai p p T V C V C V C M 1 1 Balance de masa del xenobiótico en el organismo: MT: cantidad total del xenobiótico presente en el organismo (mg); Cp: conc. del xenobiótico disuelto en la fase acuosa del plasma; Vp: volumen de la fase acuosa del plasma (CpVp es la cantidad libre).
- 22. El primer sumatorio es la cantidad de xenobiótico unido a componentes de la sangre y el segundo sumatorio es la cantidad de xenobiótico en los tejidos. = = + + = k j bj n i ai p d V V V V 1 1 Volumen de distribución:
- 23. = = = = n i i i n i i d C M V V 1 1 En los sistemas de n compartimentos se utiliza: Volumen de distribución extrapolado: 0 C Dósis V iv dext =
- 24. Aclaramiento •Es el cociente entre la velocidad de eliminación de un compuesto en un fluido de referencia, normalmente plasma sanguíneo, y su concentración en ese mismo fluido. •Tiene dimensiones de caudal. •Varios órganos pueden contribuir al aclaramiento total, por lo que se escribe como: ... + + + = i h r Cl Cl Cl Cl
- 25. x iv x iv AUC Dósis Cdt Dósis Cl → = = 0 0 •Es la medida de la capacidad de un organismo para liberarse de los xenobióticos y permite evaluar la acumulación experimentada por un compuesto tras su administración.
- 26. Biodisponibilidad •El grado de absorción en los tejidos de un xenobiótico se puede evaluar experimentalmente comparando la cantidad total de compuesto en el plasma cuando es administrado por dos vías distintas. Esto se hace a través del índice de biodisponibilidad. iv 0 oral 0 x oral x iv oral vía AUC Dósis AUC Dósis IB → → =
- 27. Modelos Fisiológicos Toxicocinéticos •Difieren en el significado y forma de obtener las ctes cinéticas utilizadas. •Las ctes cinéticas de los MF representan de entrada procesos biológicos, sobre los que se formula el propio modelo. •Permiten calcular la evolución en el tiempo de la concentración de un compuesto en un determinado órgano o tejido.
- 28. •Se adaptan fácilmente al estudio de regímenes de dosificación complicados. •Fácilmente incorporan cinéticas complejas, más realistas en la descripción de procesos naturales. •Pueden utilizarse en distintas especies. •Modelos útiles para realizar extrapolaciones (dósis, exposiciones). •Tienen como desventaja que requieren un número elevado de parámetros no siempre bien conocidos.
- 29. •Constan de una serie de compartimentos relacionados entre si mediante procesos físicos o bioquímicos.Cada compartimento representa un órgano o tejido. •Se formula mediante la realización de un balance de masa del xenobiótico en cada uno de los compartimientos. •La variación de la conc. en el tiempo en cada compartimiento genera una ec. diferencial, produciendo al final un sistema de ecuaciones a resolver.
- 31. •La resolución de dicho sistema requiere del conocimiento de una serie de parámetros y condiciones. •Cada modelo es específico para cada compuesto. •Todos los compartimientos constan en principio de tres unidades o subcompartimientos: •Espacio vascular: a través del cual se prod. el riego sanguíneo. •Espacio intersticial: entre las células.
- 33. Parámetros de los MFT •Necesarios para describir las características de los compartimientos, el comportamiento de los compuestos químicos y las interrelaciones entre los compartimentos. •No son fáciles de obtener. •Consisten principalmente en parámetros de tipo: •Anatómicos •Fisiológicos •Cinéticos y termodinámicos •De Transporte
- 34. Parámetros Anatómicos •Especifican el volumen (tamaño) del compartimiento. Parámetros Fisiológicos •Flujo sanguíneo (determina el mov. del xenobiótico entre los compartimientos). •Gasto cardiaco. •Tasa de ventilación pulmonar.
- 35. Parámetros Cinéticos y Termodinámicos •Ecuaciones cinéticas en las que intervienen constantes de velocidad para diferentes procesos. •Efecto de la temperatura sobre las velocidades de rxn. •Involucran la relación entre xenobiótico libre o asociado.
- 36. Parámetros de Transporte •Mecanismos por los cuales se da el transporte a través de las membranas biológicas (como la difusión pasiva).