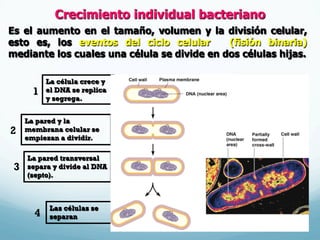
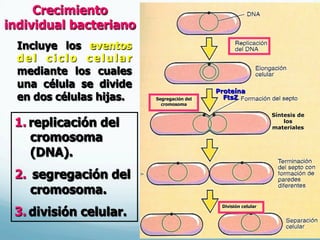
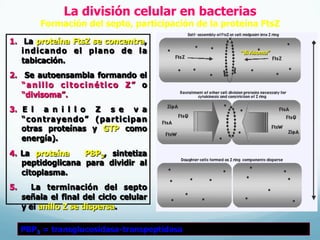
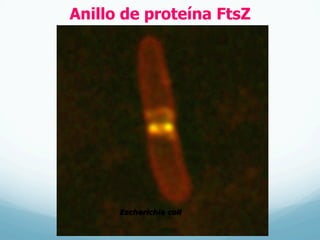
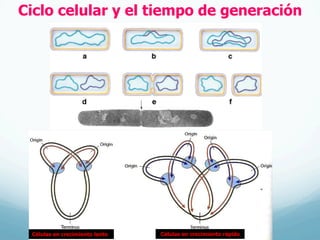
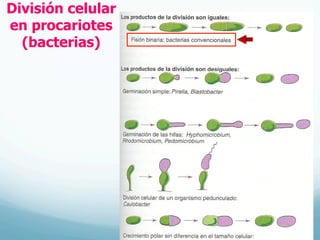
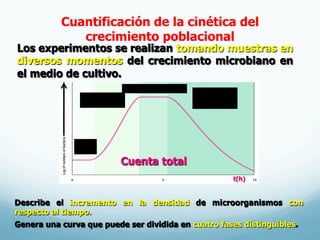
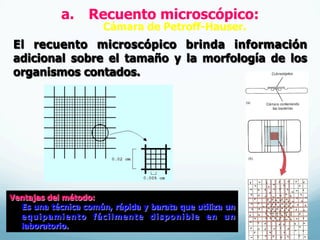
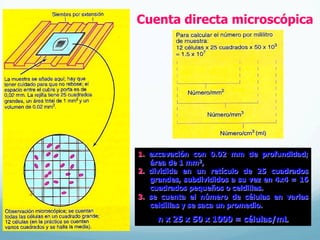
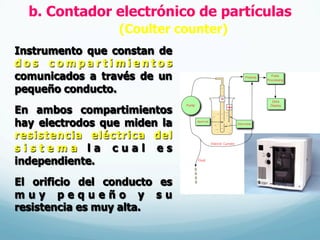
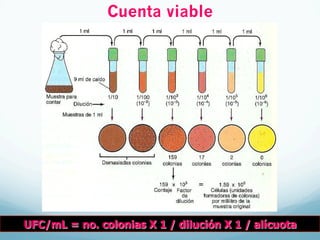
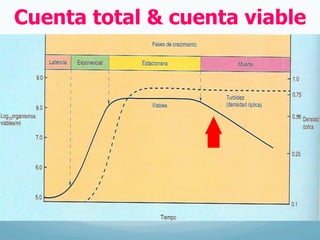
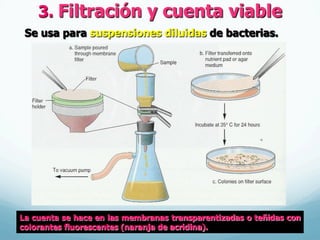
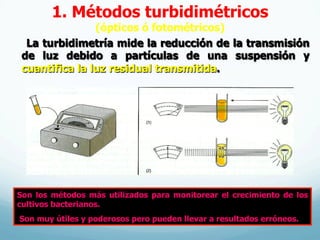
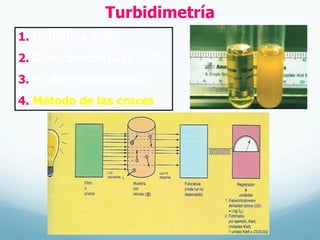
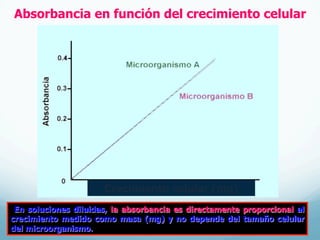
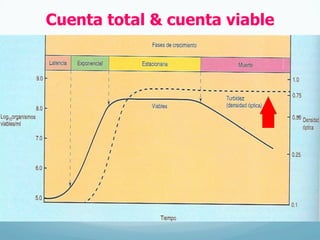
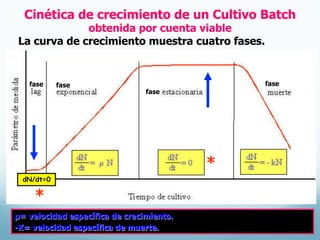
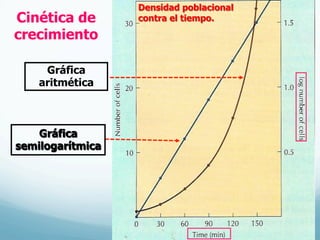
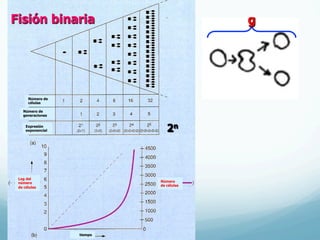
El documento describe el crecimiento microbiano en organismos unicelulares. Explica que el crecimiento se define como el aumento ordenado de todos los constituyentes celulares y resulta en un crecimiento exponencial del número de células a medida que se dividen por fisión binaria. También describe métodos para cuantificar la cinética del crecimiento poblacional como recuentos directos, viables y métodos indirectos como la turbidimetría.


































![CRECIMIENTO BALANCEADO = EQUILIBRADO
Una población de bacterias que se encuentre en
un medio adecuado en el que se mantienen
constantes todos sus parámetros nutricionales y
ambientales, crece de forma tal que:
ΔM/M = ΔN/N = Δ[ADN]/[ADN] = Δ[proteínas]/[proteínas] = ... = K
“Todos los componentes celulares
aumentan una misma proporción
por unidad de tiempo”.](https://image.slidesharecdn.com/qlzbj2ryt7uo4t2cypor-signature-c16b6408176a2255dd8961acd81903f4d3744c1919174952f1233d56a2201a7f-poli-191202050335/85/Crecimiento-microbiano-55-320.jpg)

















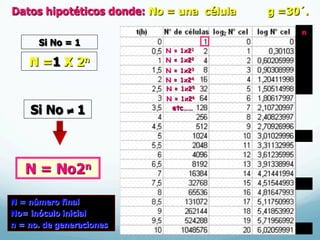





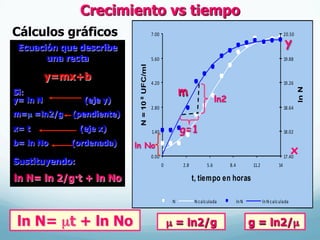



















![No glu= 5.5X106
Nglu = No gli=?
Ngli= 8.08 X109
[glu]= 0.25 g/L
[gli]= ?
gglu=140 min
ggli=145 min
28h 30 min
Tiempo total del experimento
Lag=?
0.9g/L 8.7X109
t glu=? t gli=?
L= ttotal- (tglu+tgli)](https://image.slidesharecdn.com/qlzbj2ryt7uo4t2cypor-signature-c16b6408176a2255dd8961acd81903f4d3744c1919174952f1233d56a2201a7f-poli-191202050335/85/Crecimiento-microbiano-110-320.jpg)
![N glu= 2.41X109
tglu= 20.97 h
tgli= 4.32 h
L= 3.21 h
[gli]= 0.27 g/L
RESULTADOS](https://image.slidesharecdn.com/qlzbj2ryt7uo4t2cypor-signature-c16b6408176a2255dd8961acd81903f4d3744c1919174952f1233d56a2201a7f-poli-191202050335/85/Crecimiento-microbiano-111-320.jpg)