Tema 16 ros
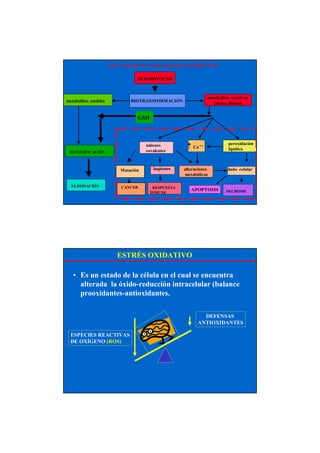
- 1. XENOBIÓTICOS BIOTRANSFORMACIONmetabolitos estables metabolitos reactivos (tóxico último) alteraciones metabólicas ELIMINACIÓN DETOXIFICACIÓN NECROSIS RESPUESTA INMUNE haptenos uniones covalentes daño celular peroxidación lipídicaCa ++ GSH MECANISMOS DE TOXICIDAD DE XENOBIÓTICOS Mutación CANCER APOPTOSIS ESTRÉS OXIDATIVO • Es un estado de la célula en el cual se encuentra alterada la óxido-reducción intracelular (balance prooxidantes-antioxidantes. ESPECIES REACTIVAS DE OXÍGENO (ROS) DEFENSAS ANTIOXIDANTES
- 2. ESPECIES REACTIVAS DE OXÍGENO • El oxígeno puede aceptar electrones para formar especies reactivas de oxígeno (ROS) tales como radicales superoxido, peroxido de hidrógeno, y radical hidroxilo. • La formación de ROS se mantiene baja gracias a los sistemas de defensa antioxidante • Alrededor de 100 enfermedades se relacionan con el estrés oxidativo y fallos en el sistema antioxidante. http://laguna.fmedic.unam.mx/mensajebioquimico/MensBioq02v26p019_Hansberg.pdf
- 5. FUENTES DE RADICALES LIBRES DE OXÍGENO EXTRACELULARES INTRACELULARES - Humo de cigarrillos - Luz solar - Oxidación de drogas (CCl4) - Radiaciones ionizantes - Shock térmico - Sustancias cíclicas de naturaleza redox (paraquat) - Transporte de electrones mitocondrial - Reacciones del complejo citocromo P450 en RE (metabolismo de xenobióticos) - Metabolismo de ácidos grasos en los peroxisomas - NADPH oxidasa de membrana (especialmente en células inflamatorias) - Subproductos de R. enzimáticas (xantina oxidasa) - Células fagocíticas Oxidación del citocromo c por acción del paraquat O2 H2O Citocromo c (Fe2+) Citocromo c (Fe3+) Cit. oxidasa (ox) (red) (I) (II)
- 6. DESTINOS MOLECULARES DEL DAÑO OXIDATIVO Oxidación de proteínas Grupos de ácidos grasos (enzimas, poliinsaturados (membranas)sistemas de transporte) Oxidación de GSH Dienos conjugados ác. Nucleicos antioxidantes Ac. Grasos hidroxilados (mutaciones, pentano, etano. transformación) Oxidación de carbohidratos (ácido hialurónico, sistema inmune) OXIDANTE
- 7. DAÑO A PROTEÍNAS Y LÍPIDOS • Proteínas: Metaloproteínas (Hb, catalasa, SOD) Presencia de insat. ó S (GA3PDH, SOD) Ca-ATPasa (Homeostasis del Ca) Proteolisis Subproductos • Lípidos insaturados: Perox. lipídica PEROXIDACIÓN LIPÍDICA Rxn R CH2CH CH CH2 COO - n 2R CH CH CH CH COO - n OOH LH L . O2 LOO R CH CH CH CH2 COO - n OH H2O INICIACIÓN O2 R CH CH CH CH2 COO - O O n PROPAGACIÓN
- 8. PEROXIDACIÓN LIPÍDICA Rxn-2 R CH CH CH CH2 COO - O OH n R CH CH CH CH2 COO - O n Fe2+ Fe3+ + OH- CH CH CH CH2 COO - O n + R
- 10. DESTINO DEL DAÑO OXIDATIVO 1. Proteínas 2. Lípidos insaturados 3. Acidos nucleicos 4. Carbohidratos (despolimerización)
- 13. La Vitamina E Ampliamente utilizada en Parkinson. Por sus propiedades liposolubles inhibe la lipoperoxidación de las membranas biológicas, estabilizándola y regulando su fluidez. Protege las estructuras celulares contra el estrés oxidativo. Inhibe significativamente la síntesis de NO.
- 14. Polyphenolics (tea, red wine, fruit, herbs/spices) Adjacent OH groups – metal binding, interferes metal absorption Chain breaking antioxidants – stop lipid peroxidation propagation Multiple phenol groups (OH on benzene) – active regions Herbal medicines ‘French Paradox’ Quercetin – apples, onions, tea Resveratrol – red wine RECOMMENDED FOR CARCINOMA PREVENTION (Federation of Obstetric & Gynaecological Societies of India) AOs in Cancer Prevention: - Antioxidant RDA Recommended Dose Possible Toxicity Level Features Causing ↑Req. Vitamin ‘A’ 5000 IU 12,500 IU Chronic intake of 125,000 IU Smoking Vitamin ‘E’ 10-20 IU 200-800 IU >1,200 IU High PUFA intake, Smoking Vitamin ‘C’ 60 mg 1000 mg Negligible / 1- 2Gms Stress, OCP,Smoking Selenium None 50-200 mg >200mg Aging, High PUFA intake, Smoking, Heavy metals
- 15. http://mimundoupa.com/media/fuentes_de_radicales_libres_y_oxidacion.jpg EL GLUTATION COMO AGENTE PROTECTOR Glutamato Acidos mercaptúricos Cisteína Acetil-CoA γ- Conjugados tioesterGlutamilcistein sintasa Glicina GSH-transferasas Glutationsintasa DEM CDNB Glutation reducido GSH H2O2 Glutation Reductasa Glutation Oxidasa NADPH GSSG 4 2H2O Glutation oxidado NADP + w 4 w EL GLUTATION COMO AGENTE PROTECTOR
- 16. Síntesis de proteínas y DNA Poder reductor del GSH Crecimiento y división celular Reacciones de reducción metabólica Síntesis de leucotrienos Regulación de enzimas-SH Resistencia a UV, Protección lente/córnea Conjugación de xenobióticos en hígado Protección celular/antioxidante PRINCIPALES FUNCIONES DE LAS CÉLULAS RELACIONADAS CON EL GSH
- 17. El Cerebro está en riesgo de sufrir daño oxidativo Daño Oxidativo Potencial •El alto uso de oxígeno y glucosa producen ERO •Alto contenido de ácidos grasos peroxidables •Áreas enriquecidas de prooxidantes como el Fe/Ascorbato Capacidad Antioxidante •Catalasa •SOD, GSH Px •GSH, Ascorbato •α-Tocoferol, Ac. Úrico H2O2, OH-, O2-, LOOH, Fe, Cu, NO, ONOO2- Especies Oxidantes Proteínas, Lípidos, Ác. Nucléicos, Metabolitos Blancos Celulares Proteínas Oxidadas, Lipoperóxidos, HNE, Cadenas rotas, 8-OHdG, Bases Oxidadas Productos de Oxidación
- 18. Reactive Nitrogen Species (RNS)Reactive Nitrogen Species (RNS) Radicals: NO. Nitric Oxide NO2 . Nitrogen dioxide Non-Radicals: ONOO- Peroxynitrite ROONO Alkyl peroxynitrites N2O3 Dinitrogen trioxide N2O4 Dinitrogen tetroxide HNO2 Nitrous acid NO2 + Nitronium anion NO- Nitroxyl anion NO+ Nitrosyl cation NO2Cl Nitryl chloride
- 20. DHEDHEDHE DHE K562NB4 DHE 0.5 µM DQA 20 µM DQA CONTROL 2 µM DQA 0.5 µM DQA 20 µM DQA CONTROL 2 µM DQA 0.5 µM DQA 20 µM DQA CONTROL 2 µM DQA 0.5 µM DQA 20 µM DQA CONTROL 2 µM DQA 0.5 µM DQA0.5 µM DQA 20 µM DQA20 µM DQA CONTROLCONTROL 2 µM DQA2 µM DQA 0.5 µM DQA 20 µM DQA CONTROL 2 µM DQA 0.5 µM DQA 20 µM DQA CONTROL 2 µM DQA 0.5 µM DQA 20 µM DQA CONTROL 2 µM DQA 0.5 µM DQA 20 µM DQA CONTROL 2 µM DQA 0.5 µM DQA0.5 µM DQA 20 µM DQA20 µM DQA CONTROLCONTROL 2 µM DQA2 µM DQA Producción de anión superóxido%MUERTECELULAR 0 20 40 60 80 100 120 0 20 40 60 80 100 120 2 µM 48 H2 µM 48 H %MURTECELULAR 0 20 40 60 80 100 120 0 20 40 60 80 100 120 20 µM 16 H20 µM 16 H DQA BSO NAC — + — + — — — — — + + + — + — + — — — — — + + + — + — + — — — — — + + + — + — + — — — — — + + + — + — + — — — — — + + + — + — + — — — — — + + + — + — + — — — — — + + + — + — + — — — — — + + + Muerte células NB4 Necrosis Apoptosis Necrosis Apoptosis butionina sulfoximina (BSO) N-acetil cisteina (NAC)
- 21. Niveles de glutation — + — + — — — — — + + + GSH(%control) 0 20 40 60 80 100 120 NB4 K562 20 µM 16 H20 µM 16 H GSH(%Control) 0 20 40 60 80 100 120 NB4 K562 2 µM 48 H2 µM 48 H DQA BSO NAC — + — + — — — — — + + + — + — + — — — — — + + + — + — + — — — — — + + + — + — + — — — — — + + + butionina sulfoximina (BSO) N-acetil cisteina (NAC)