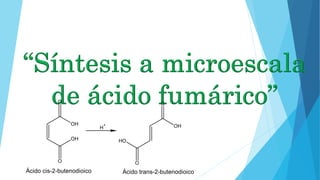
Seminario síntesis a microescala de ácido fumárico.
- 1. OH OH O O OH O OH O H + Ácido cis-2-butenodioico Ácido trans-2-butenodioico
- 2. Objetivos 1. Llevar a cabo una reacción de isomerización para convertir un isómero “cis” en un isómero “trans”. 2.- Diferenciar los isómeros geométricos del ácido 2- butenodioico mediante pruebas fisicoquímicas. 2 [Internet]. 2017 [citado 28 /04/ 2017]. Disponible en: http://es.slideshare.net 03 Las Biomoleculas
- 3. ¿Qué es una reacción de isomerización? Es una reacción en la que se produce un reordenamiento de los enlaces o la interconversión de grupos funcionales. 3 Isomerización | Tipos de reacciones Químicas [Internet]. Jaime.gia.ec. 2017 [citado 28 /04/ 2017]. Disponible en: http://jaime.gia.ec/IMS/tiposreacciones/isomerizacin1.html
- 4. ¿Qué es un isómero? Son compuestos que presentan la misma fórmula molecular, pero propiedades físicas y/o químicas distintas. 4 Bruice P. Y. Fundamentos de Química Orgánica. Primera edición. Editorial Pearson Educación. México (2007). Página 200.
- 5. Clasificación de isómeros Constitucionales Estereoisómeros 5 Bruice P. Y. Fundamentos de Química Orgánica. Primera edición. Editorial Pearson Educación. México (2007). Página 201.
- 6. Isómeros constitucionales De cadena De posición De función 6 Bruice P. Y. Fundamentos de Química Orgánica. Primera edición. Editorial Pearson Educación. México (2007). Página 201.
- 7. De cadena 7 Casillas n, Casillas n, perfil V. ISOMEROS [Internet]. Netocasillas.blogspot.mx. 2017 [citado 28/04/2017]. Disponible en: http://netocasillas.blogspot.mx/2011/12/isomeros.html Rosso. Isomería [Internet]. Es.slideshare.net. 2017 [citado 29/04/2017]. Disponible en: https://es.slideshare.net/verorosso/isomera-2530134
- 8. De grupo funcional 8 Rosso. Isomería [Internet]. Es.slideshare.net. 2017 [citado 29/04/2017]. Disponible en: https://es.slideshare.net/verorosso/isomera-2530134 Javier Santos M. Isomería estructural, conformacional y configuracional - Monografias.com [Internet]. Monografias.com. 2017 [citado 27/04/2017]. Disponible en: http://www.monografias.com/trabajos93/isomeria-quimica/isomeria-quimica.shtml
- 9. De posición 9 Rosso. Isomería [Internet]. Es.slideshare.net. 2017 [citado 29/04/2017]. Disponible en: https://es.slideshare.net/verorosso/isomera-2530134 Javier Santos M. Isomería estructural, conformacional y configuracional - Monografias.com [Internet]. Monografias.com. 2017 [citado 27/04/2017]. Disponible en: http://www.monografias.com/trabajos93/isomeria-quimica/isomeria-quimica.shtml
- 10. Estereoisómeros Ópticos Geométricos 10 DiasterómerosEnantiómeros Cis y Trans E y Z Bruice P. Y. Fundamentos de Química Orgánica. Primera edición. Editorial Pearson Educación. México (2007). Página 201.
- 11. Estereoisómeros ópticos Diastereoisómeros: Los estereoisómeros que no son imágenes especulares entre sí. 11 Bruice P. Y. Fundamentos de Química Orgánica. Primera edición. Editorial Pearson Educación. México (2007). Página 202.
- 12. Enantiómeros: Los estereoisómeros que son imágenes especulares entre sí. Pueden ser quirales o aquirales. 12 Bruice P. Y. Fundamentos de Química Orgánica. Primera edición. Editorial Pearson Educación. México (2007). Página 204.
- 13. Enantiómero quiral y aquiral 13 Bruice P. Y. Fundamentos de Química Orgánica. Primera edición. Editorial Pearson Educación. México (2007). Página 202.
- 14. Ejercicio: 14
- 15. 15 15 Pseudoefedrina Efedrina Agente farmacológico indicado para tratar la congestión nasal Provoca reacciones secundarias muy severas e incluso ataques cardiacos y derrames cerebrales
- 16. 16 (S)-talidomida (R)-talidomida Enantiómero activoProduce malformaciones en los bebés • David Palomas. El enantiómero bueno, el feo y el malo. [Internet]. [Fecha de actualización: 10/12/2012; Fecha de consulta 29/04/2017] Disponible en: http://dciencia.es/el-enantiomero-bueno-el-feo-y-el-malo/
- 17. Isomería E-Z Se utiliza en átomos tri y tetrasustituidos. Si los dos sustituyentes de número atómico más alto están del mismo lado del doble enlace se trata del isómero Z (del alemán, zusammen) y si se encuentran de distinto lado se trata del isómero E (del alemán, entgegen) 17 Estereoisómeros geométricos Isomería 2 [Internet]. quimica2bac. 2017 [citado 29/04/2017]. Disponible en: https://quimica2bac.wordpress.com/2011/02/01/isomeria-2/
- 18. 18 Isomería 2 [Internet]. quimica2bac. 2017 [citado 29/04/2017]. Disponible en: https://quimica2bac.wordpress.com/2011/02/01/isomeria-2/
- 19. Isómeros Cis y Trans 19 Bruice P. Y. Fundamentos de Química Orgánica. Primera edición. Editorial Pearson Educación. México (2007). Página 201. Trans • Los hidrógenos están del lado opuesto del doble enlace. Cis • Los hidrógenos están en el mismo lado del doble enlace.
- 20. 20
- 21. 21
- 22. 22
- 23. 23 • Isomería de compuestos orgánicos y biológicos. [Internet]. [Fecha de consulta 29/04/2017] Disponible en: http://bd.unsl.edu.ar/download.php?id=939
- 24. 24 • Cabanillas Lomelí M. L. Niveles dietéticos de ácidos trans. [Internet]. [Fecha de actualización: 24/11/2009; Fecha de consulta 29/04/2017] Disponible en: http://www.consumer.es/seguridad-alimentaria/ciencia-y-tecnologia/2005/09/14/19980.php Ácido elaídico Ácido oleico
- 25. 25
- 26. Propiedades fisicoquímicas 26 Propiedades Ácido Maléico Ácido Fumárico Fórmula C4H4O4 C4H4O4 P.m. g/Mol 116 116 P. Fusión °C 131-139 286 Solubilidad en agua a 25°C g/100mL 79 0.7 pH 1.6 3.5 pka1 1.9 3.0 pka2 6.5 4.0 Rf (fase estacionaria: sílica gel, fase móvil: acetato de etilo-acido acético(7:3)) 0.64 0.70 http://www.gtm.net/images/industrial/a/ACIDO%20FUMARICO.pdf http://www.gtm.net/images/industrial/a/ACIDO%20MALEICO.pdf
- 27. 27
- 28. Polaridad y solubilidad 28 µ≠0 µ=0
- 29. Cromatografía 29 Fase estacionaria: Sílica gel. Fase móvil: Acetato de etilo-ácido acético (7:3) Ácido maléico Rf=0.64 Ácido fumárico Rf=0.70
- 30. Interacciones moleculares y pKa 30
- 31. 31 Ácido fumárico Acidez parecida Acidez parecida Interacciones moleculares y pKa Pka1= 3.0 Pka2= 4.0
- 33. Punto de fusión 33 Ácido fumárico
- 34. 34
- 36. Reacciones sobre el doble enlace 36 Adición de bromo: • Bruice P. Y. Química Orgánica. Quinta edición. Editorial Pearson Educación. México (2008). Página 176.
- 37. Reacciones sobre el doble enlace 37 Reacción de Baeyer:
- 38. Usos del ácido maléico Se emplea en la fabricación de resinas sintéticas y en síntesis orgánicas, actúa como conservante de aceites y grasas y sus sales se utilizan en la tinción de algodón, lana y seda. 38 https://www.ecured.cu/%C3%81cido_maleico
- 39. Usos del acido fumárico Ácido de origen natural que requieren los seres humanos y los animales para vivir. Es acidulante, no higroscópico, antimicótico y antimicrobial. 39 https://www.ecured.cu/%C3%81cido_fum%C3%A1rico
- 40. 40
- 41. Ácido maléico Fórmula: C4H4O4 P.m. : 116 g/mol Punto el fusión: 131- 139 °C (desc.) Solubilidad en el agua a 25 °C: 79 g/L Pka 1: 1.9 Pka 2: 6.5 41 http://www.gtm.net/images/industrial/a/ACIDO%20MALEICO.pdf
- 42. Ácido clorhídrico Fórmula: HCl P.m. : 36.46 g/mol Punto el fusión: -25 °C Punto de ebullición: 85 °C Densidad: 1.19 g/mL Presión de vapor: 20 hPa Solubilidad: miscible con el agua 42 http://www.uacj.mx/IIT/CICTA/Documents/Acidos/Acido%20Clorhidrico.pdf
- 43. Ácido fumárico Fórmula: C4H4O4 P.m. : 116 g/mol Punto el fusión: 286 °C Solubilidad en el agua a 25 °C: 0.7 g/L Pka 1: 3.0 Pka 2: 4.0 43 http://www.gtm.net/images/industrial/a/ACIDO%20FUMARICO.pdf
- 44. Acetato de etilo Fórmula: CH3COOCH2CH3 P.m. : 88.1 g/mol Punto el fusión: -84.15°C Punto de ebullición: 70-78 °C Densidad: 0.896 g/mL Presión de vapor: 98.30 hPa a 20 °C Punto de inflamación: -4 °C Solubilidad: 80 g/L en agua a 20 °C. Miscible en hidrocarburos, cetonas y esteres. 44
- 45. Ácido acético Fórmula: CH3COOH p.m. : 60.1 g/mol Punto el fusión: 16.7 °C Punto de ebullición: 118 °C Densidad: 1.05 g/mL Presión de vapor: 15,4 mbar a 20 °C Punto de inflamación: 39 °C Solubilidad: Miscible en agua 45 http://sct.uab.cat/l-amb-controlat/sites/sct.uab.cat.l-amb- controlat/files/CH3COOH.pdf
- 46. Magnesio Fórmula: Mg° P.m. : 24.31 g/mol Punto el fusión: 651 °C Punto de ebullición: 1107 °C Densidad: 1.75 g/cm3 46 http://www.merckmillipore.com/MX/es/product/Magnesio-en-cinta,MDA_CHEM-
- 47. Bromo 47 • Fórmula: Br2 • P.M. : 159.8 g/mol • Punto el fusión: -7.2 °C • Punto de ebullición: 58.8 °C • Densidad: 3.2 g/mL • Presión de vapor: 5800 Pa a 6.85 °C • Solubilidad: 4 g/L en agua a 20 °C http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/FISQ/Ficheros/101a200/nspn0107.pdf
- 48. Tetracloruro de carbono 48 • Fórmula: CCl4 • P.M. : 153.8 g/mol • Punto el fusión: -23 °C • Punto de ebullición: 77 °C • Densidad: 1.595 g/mL • Presión de vapor: 91 mmHg a 20 °C • Solubilidad: muy poco soluble en agua http://web.ssaver.gob.mx/citver/files/2016/06/Ficha-Seguridad-Qu%C3%ADmica-Tetracloruro-de-Carbono.pdf
- 49. Permanganato de potasio Fórmula: KMnO4 p.m. : 158.034 g/mol Punto el fusión: 50 °C Punto de ebullición: >240 °C Densidad: 2.70 g/mL Presión de vapor: <0,01 mbar(20 °C) Solubilidad: 65 g/L en agua a 20 °C 49 http://www.gtm.net/images/industrial/p/PERMANGANATO%20DE%20POTASIO.pdf
- 50. 50
- 51. Síntesis 51 Adaptar un refrigerante en posición de reflujo Dejar enfriar un poco Determinar el punto de fusión del crudo de reacción En el matraz de reacción verter 3 mL de la disolución al 40% de acido maléico Calentar la mezcla durante 30 min a reflujo moderado Llevar a una filtración a vacío Verter la mezcla en un vaso de precipitados con agua-hielo Adicionar lentamente 2 mL de HCl concentrado Evitar contacto con la piel e inhalación Dejar secar Calcular rendimiento Realizar pruebas fisicoquímicas
- 52. 52
- 53. Síntesis 53 Adaptar un refrigerante en posición de reflujo Dejar enfriar un poco Determinar el punto de fusión del crudo de reacción En el matraz de reacción verter 3 mL de la disolución al 40% de acido maléico Calentar la mezcla durante 30 min a reflujo moderado Llevar a una filtración a vacío Verter la mezcla en un vaso de precipitados con agua-hielo Adicionar lentamente 2 mL de HCl concentrado Evitar contacto con la piel e inhalación Dejar secar Calcular rendimiento Realizar pruebas fisicoquímicas
- 54. Observar solubilidad 54 Colocar 0.01 g de ácido maléico en un tubo de ensayo y 0.01 g de ácido fumárico en otro Adicionar 1 mL de agua a cada tubo Agitar Solubilidad
- 55. 55 Observar y registrar los pH Observar Se prepara una cámara con Acetato de etilo-ácido acético (7:3) Introducir la placa Ácido acético Observar, obtener los valores de Rf y compararlos con los de la literatura. Tomar una alícuota y colocarla en la placa Introducir una tira de pH pH Cromatografía Reacción con Mg° Adicionar un trozo de cinta de magnesio a cada tubo
- 56. 56 Identificación de insaturaciones Observar, registrar tiempo de reacción y coloración Colocar 0.01 g de ácido maléico en un tubo de ensayo y 0.01 g de ácido fumárico en otro Adicionar una gota de permanganato Adicionar una gota de bromo a cada tubo Reacción de Baeyer Colocar 0.10 g de ácido maléico en un tubo de ensayo y 0.01 g de ácido fumárico en otro Observar, registrar tiempo de reacción y coloración Agitar Agitar Adición de halógenos
