Guia de atomo decimo 2021 convertido
•
0 recomendaciones•777 vistas
Guia decimo
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Copia de bloque ii aprendizajes 14%2c15 y 16 copia

Copia de bloque ii aprendizajes 14%2c15 y 16 copia
Hibridación del Carbono y Características de los Enlaces Covalentes

Hibridación del Carbono y Características de los Enlaces Covalentes
Similar a Guia de atomo decimo 2021 convertido
Similar a Guia de atomo decimo 2021 convertido (20)
Más de mariadel213
Más de mariadel213 (20)
Último
Centros Multigrados Procedimientos para la planificación en los Centros Educativos tipo V ( multi...

Procedimientos para la planificación en los Centros Educativos tipo V ( multi...Katherine Concepcion Gonzalez
Último (20)
Prueba de evaluación Geografía e Historia Comunidad de Madrid 2º de la ESO

Prueba de evaluación Geografía e Historia Comunidad de Madrid 2º de la ESO
Prueba libre de Geografía para obtención título Bachillerato - 2024

Prueba libre de Geografía para obtención título Bachillerato - 2024
EL HABITO DEL AHORRO en tu idea emprendedora22-04-24.pptx

EL HABITO DEL AHORRO en tu idea emprendedora22-04-24.pptx
Tema 10. Dinámica y funciones de la Atmosfera 2024

Tema 10. Dinámica y funciones de la Atmosfera 2024
Procedimientos para la planificación en los Centros Educativos tipo V ( multi...

Procedimientos para la planificación en los Centros Educativos tipo V ( multi...
2 REGLAMENTO RM 0912-2024 DE MODALIDADES DE GRADUACIÓN_.pptx

2 REGLAMENTO RM 0912-2024 DE MODALIDADES DE GRADUACIÓN_.pptx
Tema 19. Inmunología y el sistema inmunitario 2024

Tema 19. Inmunología y el sistema inmunitario 2024
BIOMETANO SÍ, PERO NO ASÍ. LA NUEVA BURBUJA ENERGÉTICA

BIOMETANO SÍ, PERO NO ASÍ. LA NUEVA BURBUJA ENERGÉTICA
Los avatares para el juego dramático en entornos virtuales

Los avatares para el juego dramático en entornos virtuales
TALLER DE DEMOCRACIA Y GOBIERNO ESCOLAR-COMPETENCIAS N°3.docx

TALLER DE DEMOCRACIA Y GOBIERNO ESCOLAR-COMPETENCIAS N°3.docx
RESULTADOS DE LA EVALUACIÓN DIAGNÓSTICA 2024 - ACTUALIZADA.pptx

RESULTADOS DE LA EVALUACIÓN DIAGNÓSTICA 2024 - ACTUALIZADA.pptx
Análisis de los Factores Externos de la Organización.

Análisis de los Factores Externos de la Organización.
Guia de atomo decimo 2021 convertido
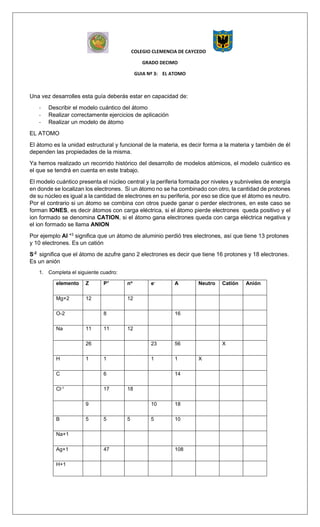
- 1. COLEGIO CLEMENCIA DE CAYCEDO GRADO DECIMO GUIA Nº 3: EL ATOMO Una vez desarrolles esta guía deberás estar en capacidad de: - Describir el modelo cuántico del átomo - Realizar correctamente ejercicios de aplicación - Realizar un modelo de átomo EL ATOMO El átomo es la unidad estructural y funcional de la materia, es decir forma a la materia y también de él dependen las propiedades de la misma. Ya hemos realizado un recorrido histórico del desarrollo de modelos atómicos, el modelo cuántico es el que se tendrá en cuenta en este trabajo. El modelo cuántico presenta el núcleo central y la periferia formada por niveles y subniveles de energía en donde se localizan los electrones. Si un átomo no se ha combinado con otro, la cantidad de protones de su núcleo es igual a la cantidad de electrones en su periferia, por eso se dice que el átomo es neutro. Por el contrario si un átomo se combina con otros puede ganar o perder electrones, en este caso se forman IONES, es decir átomos con carga eléctrica, si el átomo pierde electrones queda positivo y el ion formado se denomina CATION, si el átomo gana electrones queda con carga eléctrica negativa y el ion formado se llama ANION Por ejemplo Al +3 significa que un átomo de aluminio perdió tres electrones, así que tiene 13 protones y 10 electrones. Es un catión S-2 significa que el átomo de azufre gano 2 electrones es decir que tiene 16 protones y 18 electrones. Es un anión 1. Completa el siguiente cuadro: elemento Z P+ no e- A Neutro Catión Anión Mg+2 12 12 O-2 8 16 Na 11 11 12 26 23 56 X H 1 1 1 1 X C 6 14 Cl-1 17 18 9 10 18 B 5 5 5 5 10 Na+1 Ag+1 47 108 H+1
- 2. 2. Realiza la distribución electrónica de los números atómicos múltiplos de siete, ¿cuál es el nombre y el símbolo químico de cada uno? Dentro de los subniveles de energía se encuentran los orbitales, en cada orbital caben dos electrones y uno de ellos gira hacia la derecha (Spin positivo 1/2), se simboliza con flecha hacia arriba y el otro gira hacia la izquierda (Spin negativo -1/2) simbolizado con flecha hacia abajo. Observa la distribución electrónica del oxígeno y del boro. 3. Realiza la distribución electrónica de Z=12 presentando diagrama de orbitales, ¿de qué elemento químico se trata? 4. Explica que significan los siguientes símbolos: 6 C 12 6C14 8 O 16 5. Dibuja un átomo de fosforo según el modelo atómico de Bohr si Z = 15 y A = 31 6. Cuál es el número atómico, el nombre y el símbolo del elemento para cada caso: A) 1s2 2s2 2p6 3s2 3p6 4s2 3d5 B) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 C) 1s2 2s2 2p6 3s2 3p3 7. ¿Qué son los isotopos? Da ejemplos Numero cuántico principal, Número cuántico secundario, Número cuántico magnético, Numero cuántico de spin. 8. A que elemento representa este modelo, ¿cuál es su símbolo químico? ¿Su Z? ¿su A? Realiza consulta acerca de sus aplicaciones industriales Esta es la distribución electrónica por niveles de energía de tres elementos: calcio, azufre y estroncio: 9. Escoge un elemento de la tabla periódica que no haya sido trabajado hasta ahora en esta guía… realiza su distribución electrónica y busca información acerca de sus usos. 10. Explica en que consiste la radioactividad. ¿Para qué se utiliza?