Acidos y bases 2018
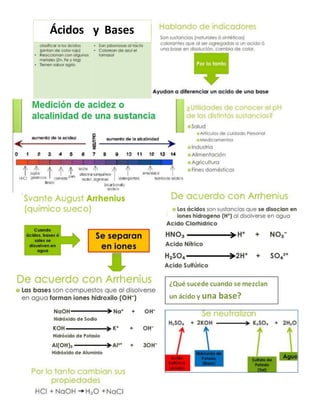
- 1. Ácidos y Bases ¿Qué sucede cuando se mezclan un ácido y una base?
- 2. ¿Pero cómo determinamos el pH? pH= - log [H+] Trabajamos con soluciones de ácidos y bases fuertes, por lo tanto, la [H+ ] = [ácido] (esto para ácidos que liberan un solo H+ sino se hacen algunos ajustes) ¿Y si es una base? Recurrimos a la escala de pOH: pOH = -log [OH- ] Y además: pH + pOH = 14 , porqueestamos en medio acuoso… ¿Cómosaberqué tan ácida esuna solución? Por laescalade pH, creadapor el químicodanés SorenPederLauriz(S.P.L.) Sorensen (Sorensen) Al investigarel efectode laconcentraciónde los ionessobre lasproteínascreóen1909 una formasimple de expresarlaconcentraciónde ionesde hidrógeno enunasolución:laescalade pH (potencial de hidrógeno). Para qué sirve el pH Sorensen diseñó la escala para medir la acidez o alcalinidad de una substancia: las soluciones que recibían valores de pH de 0 eran las más ácidas, las de 14 las más alcalinas. Para eso,El pH de algunas disoluciones comunes Directamente: con un indicador ácido-base: sustancia que cambian de color según la acidez del medio. Indirectamente: si sabemos la concentración molar (mol/L) de catión hidrógeno, utilizamos la fórmula: La escala de pH se usa para clasificar soluciones en términos de su acidez o alcalinidad (qué tan básica es). Puesto que la escala está basada en valores de pH, es logarítmica, lo que significa que un cambio en una unidad de pH corresponde a un cambio diez veces mayor en la concentración de iones H+. A menudo se dice que la escala de pH va de 0 a 14 y la mayoría de las soluciones entran en este rango, sin embargo es posible encontrar soluciones con pH menor a 0 o mayor a 14. Cualquier valor menor a 7.0 es ácido y cualquier valor mayor a 7.0 es básico o alcalino. El pH dentro de las células humanas (6.8) y el de la sangre (7.4) son muy cercanos al neutro. Los valores de pH extremos, por arriba o por debajo de 7.0, generalmente se consideran desfavorables para la vida. Sin embargo, el ambiente dentro de tu estómago es muy ácido, con un pH de entre 1 y 2
- 3. Piensay explica: 1.Si una pera tiene pH de 3 y una banana de 5, ¿cuál de ellas es más ácida? 2.Los morrones tienen pH de 4,3 y los huevos frescos de 7,8.¿Cuál de estos alimentos es más ácido y cuál más básico? 3.Observando la escala de pH, responde: a..La leche tiene pH de 6,4, es ácida o básica b..Un jabón tiene pH de 10,3, es ácido o básico? c..Un refresco tiene pH de 3 y la orina humana de 6. ¿Cuántas veces es más ácido el refresco? d..Al aumentar el pH de una solución, ¿la hacemos más o menos básica? 4..Al disminuir el pH de una solución, ¿la hacemos más o menos ácida? 5.a) Clasifica las sustancias de acuerdo a la definición de Arrhenius: KOH, HNO3, Al (OH)3 HCl b) Representa la escala de pH y señala en ella, dónde se encontrarían los valores de pH para soluciones acuosas 0,25 M de DOS de las sustancias anteriores. 6..Un frasco contiene una solución acuosa de algo sin identificar. Parte de su etiqueta dice: 0,45 M. Realizas una prueba con papel indicador y resulta ser una base. ¿Cuál es su pOH y la concentración molar de ion OH- ? 7..Calcula el pH y el pOH de una solución 0,15 M de un ácido fuerte de fórmula H2X. 8..Calcula: la concentración de H+ de la solución de HNO3 0,95 M.