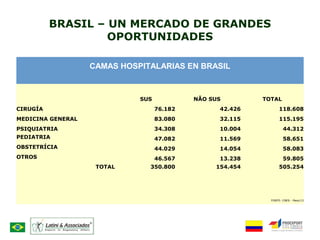
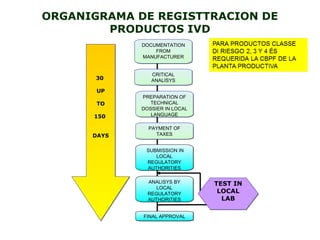
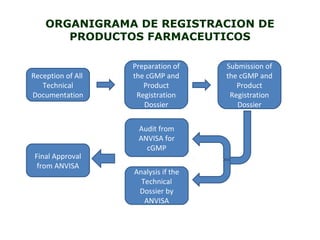
Este documento proporciona información sobre el mercado regulatorio de Brasil. Resume que Brasil es un gran mercado con 196 millones de habitantes y cuenta con un sistema estructurado de asuntos regulatorios. Describe brevemente el proceso de registro de empresas y productos médicos, odontológicos, IVD y cosméticos en Brasil, incluidos los documentos requeridos y los tiempos de aprobación típicos.