Agua (1).ppt
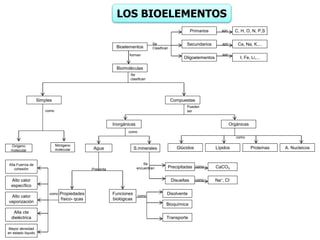
- 1. Bioelementos I, Fe, Li,... Ca, Na, K,... C, H, O, N, P,S Oligoelementos Secundarios Primarios Se Clasifican son son son Biomoléculas forman Simples Compuestas Oxígeno molecular Nitrógeno molecular Lípidos Glúcidos S.minerales Agua Orgánicas Inorgánicas A. Nucleicos Proteínas Pueden ser como como Se clasifican como Propiedades físico- qcas Funciones biológicas Mayor densidad en estado líquido Alta cte dieléctrica Alto calor vaporización Alto calor específico Alta Fuerrza de cohesión Disolvente Bioquímica Transporte Presenta como como Se encuentran Disueltas Precipitadas Na+, Cl- CaCO3 como como LOS BIOELEMENTOS
- 2. Agua 60% El término líquido corporal hace referencia al agua corporal y a las sustancia disueltas en ella. Los líquidos son responsables del 60% del peso corporal del cuerpo El agua es el principal e imprescindible componente del cuerpo humano. El ser humano no puede estar sin beberla más de cinco o seis días sin poner en peligro su vida. • El porcentaje de agua en un hombre adulto es cerca del 60% de su peso corporal (un hombre de 70 Kg. contiene 42 litros de agua). Este porcentaje varía de persona a persona de acuerdo a la edad, el sexo y el contenido de tejido adiposo. Sexo Edad (años) Hombres Mujeres Recién Nacido 80 75 1-5 65 65 10-16 60 60 17-39 60 50 40-59 55 47 60 a más 50 45
- 3. Tejido % de H2O % de peso corporal Litros H2O / 70 kg Piel 72.0 18.0 9.07 Músculo 75.6 41.7 22.1 Esqueleto 22.0 15.9 2.45 Cerebro 74.8 2.0 1.05 Hígado 68.3 2.3 1.03 Corazón 79.2 0.5 0.28 Pulmones 79.0 0.7 0.39 Riñones 82.7 0.4 0.25 Bazo 75.8 0.2 0.10 Sangre 83.0 8.0 4.65 Intestino 74.5 1.8 0.94 Tejido adiposo 10.0 ~ 10.0 0.70 Existe gran variabilidad en la proporción de agua en los distintos tejidos. Así los tejidos más jóvenes y más activos desde el punto de vista metabólico presentan una proporción más elevada. Por el contrario, en los tejidos envejecidos y poco activos la proporción disminuye considerablemente.
- 4. 1. COMPARTIMENTACION ACUOSA CORPORAL El agua corporal (líquido corporal) está dividida en aquella que está localizada dentro de las células (líquido intracelular) y la localizada fuera de ella (líquido extracelular). El líquido intracelular constituye aproximadamente un 55% del peso corporal de agua existente en el organismo (cerca de 23 litros, en hombre de 70 kg). El líquido extracelular constituye aproximadamente 45% del total de peso corporal de agua (cerca de 19 litros) Compartimento de líquidos corporales (hombre de 70 Kg). % de peso corporal % del total de agua corporal Volumen (litros) Líquido extracelular (LEC) 27 45 19.0 - Plasma 4.5 7.5 3.2 - Líquido intersticial 12.0 20.0 8.4 - Tejido conectivo denso 4.5 7.5 3.2 - Hueso 4.5 7.5 3.2 - Transcelular 1.5 2.5 1.0 Líquido intracellular (LIC) 33 55 23.0 Total de agua corporal 60% 100% 42 litros
- 5. LIQUIDO INTRACELULAR (LIC) El líquido intracelular, puede dividirse a su vez en: - El agua libre (95%), es usada como medio dispersante del sistema coloidal del protoplasma, como el agua de tejidos y líquidos corporales. - El agua ligada (4-5%), comprende el agua inmovilizada dentro de las estructuras fibrosas de las macromoléculas. Se encuentra en constante movimiento. Es transportado rápidamente por la sangre. Contiene nutrientes para el mantenimiento de la vida celular El catión fundamental es el ion K+, y los dos aniones dominantes son los fosfatos orgánicos (PO4 3-) y los aminoácidos con carga negativa de las proteínas. H20
- 6. LÍQUIDO EXTRACELULAR (LEC) * Está localizado en varios compartimentos. - Agua plasmática (plasma y linfa), que es cerca del 7.5% (3.2 L) del total de agua corporal. - Líquido intersticial, que es cerca del 20.0% (8.4 L) del total de agua corporal. - Líquido transcelular, comprende casi el 2.5% (1L) del total de agua corporal. Ejem: líquido cefalorraquídeo en el cerebro, las secreciones digestivas, líquido intraocular, líquido sinovial en articulaciones, líquido pericárdico, pleural y peritoneal entre las membranas serosas. - Además, hay agua extracelular localizada en el tejido conectivo denso y el hueso (3,2 L c/u). * El catión fundamental es el Na+ y el anión principal es el Cl-.
- 7. 2. INGESTA Y EXCRECION DE AGUA EN EL HOMBRE Alimento % agua Alimento % agua Gelatina seca 13 Carne de trenera 66 Mantequilla 20 Papas 80 Pan 36 Naranjas 86 Queso 36 a 50 Leche 87 Carne de res 47 Espárrago 92 Jamón 58 Lechuga 96 Pollo 63 Pepino 96
- 8. 3. ESTRUCTURA MOLECULAR • La estructura tridimensional de la molécula de agua es un tetraedro irregular con el oxígeno en el centro. Los dos enlaces con el hidrógeno se dirigen hacia las dos esquinas del tetraedro, en tanto que los electrones no compartidos ocupan las dos esquinas restantes. • El ángulo entre los 2 átomos de H es de 104.5°. • Debido a su estructura tetraédrica asimétrica, la carga eléctrica no se distribuye de modo uniforme. El lado del oxígeno, es relativamente abundante en electrones, en tanto que el núcleo del hidrógeno relativamente descubierto forma una región de carga positiva. • El término “dipolo” denota que la molécula de agua, possee carga eléctrica (electrones) distribuida de modo desigual en su estructura. () () () ()
- 9. • Los enlaces de hidrógeno dan a las moléculas de agua propiedades de: Adhesion y cohesion. Tensión superficial, que permite al agua formar capas, adherirse a superficies o lubricar superficies. Permitir al agua resistir cambios de temperatura. Enlaces de hidrógeno () () () () (+) (+) (+) (+) • La polaridad de la molécula de agua causa que ésta presente “enlaces de hidrógeno intramoleculares”. • Los enlaces de hidrógeno (puente de H) resultan de la interacción electrostática entre un hidrógeno de un dipolo hídrico y el par de electrones no compartidos de otro dipolo hídrico. • Los enlaces de hidrógeno son débiles respecto a los enlaces covalentes. • Los enlaces de hidrógeno son importantes porque estabilizan la estructura tridimensional de proteínas y ácidos nucleicos
- 10. 4.1. ELEVADA CONSTANTE DIELÉCTRICA Las moléculas de agua se oponen a la atracción electrostática entre los iones + y -, debilitando dichas fuerzas de atracción. El agua posee una de las constantes dieléctricas más altas (K= 80 a 20°C) y esta gran capacidad para reducir la fuerzas de atracción entre partículas cargadas le ha dado el reconocimiento de disolvente universal. La molécula de agua que rodea a los iones se orienta de manera que sus polos positivos están dirigidos hacia los aniones y los negativos hacia los cationes. 4. PROPIEDADES FISICAS Y QUIMICAS DEL AGUA
- 11. 4.2. ELEVADA TENSIÓN SUPERFICIAL El agua tiene una alta tensión superficial debido a la cohesión de sus moléculas; éstas se atraen entre sí con mayor fuerza que las moléculas del aire. Las moléculas de agua presentan fuerzas de atracción en todas direcciones hacia las moléculas circundantes, sin embargo, como en la superficie ya no hay más moléculas de agua, las moléculas de agua de esta zona no están sujetas a fuerzas de atracción semejantes en todas direcciones y tienden a aglutinarse más en esta parte que en otras zonas del líquido. La tensión generada en el sistema respiratorio es una resistencia para la respiración, ya que a través de la pared del alvéolo debe realizarse el intercambio gaseoso. Las células epiteliales alveolares tipo II secretan el surfactante pulmonar (dipalmitoil lecitina), una sustancia que disminuye la tensión superficial dentro de los alvéolos.
- 12. 4.3. CAPILARIDAD Las fuerzas de adhesión y cohesión explican la tendencia del agua a ascender por los tubos de calibre muy pequeño. Las fuerzas de adhesión atraen las moléculas de agua hacia los grupos cargados presentes en las superficies del tubo. Luego, otras moléculas presentes en el interior del tubo son "arrastradas" por las fuerzas de cohesión. Gracias a la capilaridad, la sangre, que en su mayor parte es agua, puede completar el ciclo circulatorio a nivel de los vasos pequeños. Adhesión Cohesión
- 13. Agua 0º 100º Metanol -98º 65º Etanol -117º 78º n-Propanol -127º 97º Acetona -95º 56º Benceno 6º 80º Cloroformo -63º 61º Punto fusión, ºC Punto ebullición, ºC 4.4. ELEVADO PUNTO DE FUSION y ELEVADA TEMPERATURA DE EBULLICION Bacterias termófilas Krill (crustaceo) que vive bajo el hielo Antartico. Esto hace que el agua se mantenga líquida en un amplio espectro de temperaturas (0 - 100°C), lo que posibilita que pueda existir vida en diferentes climas, incluso a temperaturas extremas
- 14. Calor específico - Cal/g °C Alcohol 0.58 Oro 0.03 Granito 0.19 Hierro 0.10 Aceite de oliva 0.47 Agua 1.00 Sustancia Calor específico 4.5. ELEVADO CALOR ESPECIFICO y ELEVADO CALOR DE VAPORIZACION Calor de vaporización - Cal/g Agua 540 Metanol 263 Etanol 204 n-Propanol 164 Acetona 125 Benceno 94 Cloroformo 59 Sustancia Calor vaporización El calor específico se refiere a la cantidad de calor necesario para elevar la temperatura de 1 g de agua, de 14.5 a 15.5°C. El calor latente de vaporización es la cantidad de energía necesaria para superar las fuerzas de atracción entre las moléculas de agua y transformarla al estado gaseoso. El H2O es un mecanismo adecuado para estabilizar la temperatura del organismo, evitando una excesiva elevación o disminución de la misma.
- 15. Baja densidad Alta densidad Hielo Agua líquida Los enlaces de H son más estables Los enlaces de H constantemente se rompen y reforman 4.6. DENSIDAD MÁXIMA A 4°C El agua se expande al tiempo que se solidifica porque los puentes de hidrógeno en las moléculas de agua del enrejado cristalino mantienen a estas moléculas lo suficientemente separadas como para dar al hielo una densidad 10% menor que la densidad del agua.
- 16. Las dos alteraciones del equilibrio hídrico son la deshidratación o depleción del volumen acuoso y la hidratación o exceso de volumen acuoso. La depleción hídrica puede deberse a una menor ingestión (ej. coma) o al incremento de la pérdida (ej. sudoración intensa, pérdida renal en la diabetes mellitas, diarrea del lactante o cólera). Las causa de exceso de agua corporal incluyen aumento de la ingestión (ej. administración excesiva de líquidos por vía intravenosa) y disminución de la excreción (ej. insuficiencia renal intensa). 5. ALTERACIONES DEL EQUILIBRIO HIDRICO ECF osmotic pressure rises Excessive loss of H2O from ECF Cells lose H2O to ECF by osmosis; cells shrink 1 2 3 H2O moves into cells by osmosis; cells swell ECF osmotic pressure falls Excessive H2O enters the ECF (a) Mechanism of dehydration (b) Mechanism of hypotonic hydration 1 2 3
- 17. 6.1. Es un excelente disolvente y medio de suspensión 6. FUNCIONES BIOQUIMICAS Y FISIOLOGICAS
- 18. Deshidratación síntesis Cortos polímeros Monómeros Hidrólisis Grandes polímeros 6.2. Participa en las reacciones químicas 5.3. Actúa como lubricante Es una parte importante de las mucosas y otros líquidos lubricantes. La lubricación es necesaria en el tórax y abdomen, donde los órganos internos se tocan, deslizándose entre sí. También es necesario en las articulaciones, donde los huesos, ligamentos y tendones se friccionan entre ellos.
- 19. 6.3. Regula la temperatura corporal El agua requiere una gran cantidad de calor para elevar su temperatura y una gran pérdida de calor para reducirla. Por tanto la existencia de una gran cantidad de agua ayuda a mantener la homeostasis de la temperatura corporal. Cuando el agua se evapora de la piel (perspiración) capta grandes cantidades de calor y proporciona un excelente mecanismo de enfriamiento. Sudor