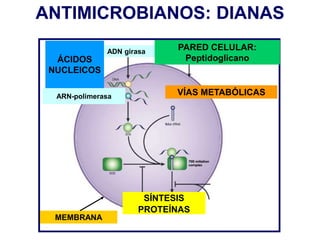
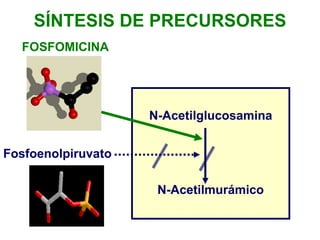
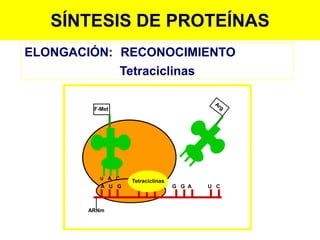
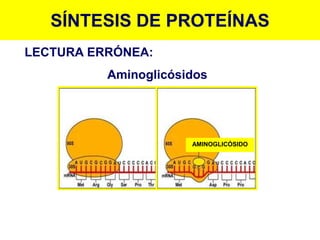
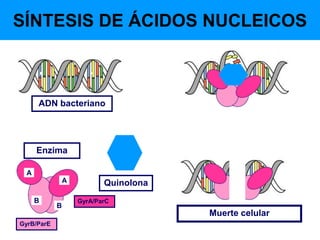
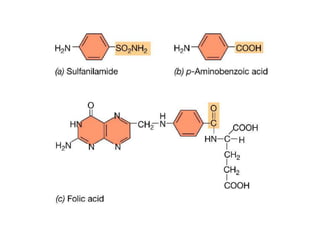
Este documento describe diferentes tipos de antimicrobianos y su mecanismo de acción. Explica que los antimicrobianos más comunes actúan inhibiendo la síntesis de la pared celular bacteriana, la síntesis de proteínas o la síntesis de ácidos nucleicos. En particular, antibióticos como las penicilinas y cefalosporinas inhiben la síntesis de peptidoglicano en la pared celular bacteriana al bloquear la transpeptidación. Otros como los aminoglucósidos y las tetraciclinas interfieren con