Este documento resume la historia de la teoría atómica desde los griegos Demócrito y Leucipo en el siglo V a.C. hasta los modelos atómicos modernos del siglo XX. Explica que los átomos fueron propuestos originalmente como partículas indivisibles de materia, luego Dalton estableció los cuatro postulados fundamentales de la teoría atómica moderna en 1808, y los modelos atómicos continuaron desarrollándose a medida que se descubrían nuevas partículas como el electrón y





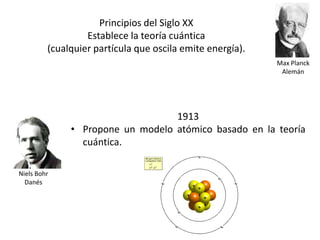
![Postulados de la teoría cuántica de Bohr
• El átomo tiene un núcleo en donde se
encuentra casi la totalidad de su masa
[protones (+) y neutrones(+ -)].
• Los electrones (-) giran alrededor del
núcleo en órbitas fijas.
• Estas órbitas se conocen como niveles de
energía.
• Las órbitas cercanas al núcleo son de baja
energía y las lejanas son de alta energía.
• Los electrones pueden cambiar de una
órbita a otra liberando o absorbiendo
energía.
• La energía que gana o pierde un electrón
se denomina “cuanto de energía”.](https://image.slidesharecdn.com/atomo-120430210247-phpapp01/85/Atomo-7-320.jpg)

