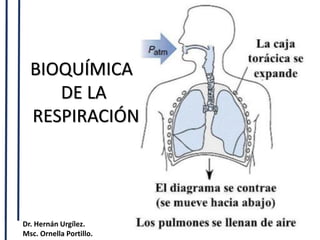
BIOQUÍMICA DE LA RESPIRACIÓN
- 1. BIOQUÍMICA DE LA RESPIRACIÓN Dr. Hernán Urgílez. Msc. Ornella Portillo.
- 4. Gases en la Tabla Periódica HELIO NITRÓGENO OXÍGENO FLÚOR CLORO HIDRÓGENO NEÓN ARGÓN KRIPTÓNXENÓN RADÓN
- 5. LEYES DE LOS GASES LEY DE DALTON "La presión total de una mezcla es igual a la suma de las presiones parciales que ejercen los gases de forma independiente” En donde P1, P2, P3,… son presiones parciales Pparcial = Xgas . Ptotal
- 6. LEYES DE LOS GASES LEY DE GRAHAM “Efusión y difusión gaseosa (Velocidades moleculares)” Fundamento Teórico • Las moléculas de los gases están en rápido movimiento. • Sus velocidades promedio son proporcionales a la temperatura absoluta. • La misma temperatura, la energía cinética promedio de las moléculas de gases diferentes es igual • V: velocidad de difusión • M: peso molecular • D1: densidad.
- 7. LEYES DE LOS GASES LEY DE AVOGADRO Descubierta por Avogadro a principios del siglo XIX Establece la relación entre la cantidad de gas y su volumen cuando se mantienen constantes la Temperatura y la Presión EL VOLÚMEN ES DIRECTAMENTE PROPORCIONAL A LA CANTIDAD DEL GAS • Si aumenta la cantidad de gas, aumenta el volumen. • Si disminuimos la cantidad de gas, el volumen disminuye. V= (𝑅𝑇) 𝑃 𝑛 𝑅𝑇 𝑃 𝑠𝑜𝑛 𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒𝑠
- 8. LEYES DE LOS GASES LEY DE GAY LUSSAC Enunciada por Joseph Louis Gay Lussac a principios de 1800 Establece la relación entre la temperatura y la presión de un gas cuando el volumen es constante • si aumentamos la temperatura, aumentará la presión • Si disminuimos la temperatura, disminuirá la presión. LA PRESIÓN DEL GAS ES DIRECTAMENTE PROPORCIONAL A SU TEMPERATURA 𝑃1 𝑇1 = 𝑃2 𝑇2
- 9. LEY DE BOYLE Fue descubierta por Robert Boyle en 1662 Establece que la presión de un gas en un recipiente fijo es inversamente proporcional al volumen del recipiente, cuando la temperatura es constante • si la presión aumenta, el volumen disminuye. • Si la presión disminuye, el volumen aumenta. EL VOLÚMEN ES INVERSAMENTE PROPORCIONAL A LA PRESIÓN LEYES DE LOS GASES P= (nRT) 1 𝑉 𝑛𝑅𝑇 𝑠𝑜𝑛 𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒𝑠.
- 10. LEYES DE LOS GASES LEY DE CHARLES En 1787, Jack Charles estudió por primera vez la relación entre el volumen y la temperatura de una muestra de gas a presión constante y observó que cuando se aumentaba la temperatura el volumen del gas también aumentaba y que al enfriar el volumen disminuía EL VOLÚMEN ES DIRECTAMENTE PROPORCIONAL A LA TEMPERATURA DEL GAS • Si la temperatura aumenta, el volumen del gas aumenta. • Si la temperatura del gas disminuye, el volumen disminuye.
- 11. LEYES DE LOS GASES ECUACIÓN DEL GAS IDEAL “Explica la relación entre las cuatro variables P, V, T y n.” P.V = n.R.T
- 12. Movimiento de los Gases en el Organismo ORGANISMO OXÍGENO DIÓXIDO DE CARBONO NITRÓGENO Sangre Arterial 1.9 % 50 % 0.9 % Sangre Venosa 13 % 56 % 0.9 % Agua en equilibrio con aire alveolar 0.3 % 2.6% 0.9 % Factores del Paso de los Gases en las Membranas Pulmonares o Celulares • Las diferencias de presión del gas entre un lado y el otro de la membrana. • Las diferencias en la capacidad de combinación de los componentes sanguíneos con el oxígeno, y el dióxido de carbono debidos al cambio del pH.
- 13. APLICACIONES EN LA MEDICINA Medición de la Presión. Hipertensión. Cámaras Hiperbáricas. Gases en la Sangre. Se fundamenta en las Leyes Físicas de los gases, que sostienen que al aumentar la presión, aumenta la solubilidad del gas (OXÍGENO) en un líquido (PLASMA SANGUÍNEO). Al proveer al cuerpo de grandes cantidades de oxígeno se establecen las funciones que se pierden cuando la cantidad es baja. Así, al aumentar 10 a 15 veces más la cantidad de oxígeno en el cuerpo, se crean varios efectos como. • La reducción de las inflamaciones. • La mejoría de la circulación sanguínea. • La aceleración de las cicatrizaciones. • La generación de nuevos vasos sanguíneos en áreas con circulación pobre. • La remodelación de los huesos dañados. • El aumento de la elasticidad, el eritrocito para favorecer la circulación en los pequeños vasos sanguíneos.
- 14. La terapia de oxigeno hiperbárico consiste en respirar oxígeno en una cámara a presión. La Administración de Alimentos y Medicamentos (FDA) ha autorizado cámaras hiperbáricas para ciertos usos médicos, como el tratamiento de la enfermedad de descompresión que sufren los buzos. APLICACIONES EN LA MEDICINA
- 15. APLICACIONES EN LA MEDICINA HIPERBARISMO Tenemos los Pulmones aproximadamente de 4 a 6 Litros llenos de aire. Desde el punto de vista físico-químico y fisiológico evalúa las modificaciones morfuncionales agudos y crónicos que se producen cuando el organismo es sometido a presiones altas. BUCEO
- 16. APLICACIONES EN LA MEDICINA CARACTERÍSTICAS DEL HIBERBARISMO • Cada 10 a 13 metros debajo del nivel del mar la presión aumenta 1 atm. • En buceo, los gases de cavidades se comprimen, el volumen se reduce y aumenta la presión. RELACION INVERSA : VOLUMEN –PRESION • En ascenso: sobre expansión pulmonar, Neumotórax. • Burbujas en Sangre. (Embolia Gaseosa) HIPOBARISMO Condición ambiental en donde la presión esta por debajo de 1 atm, por lo tanto un individuo no adaptado puede presentar pequeñas o severas alteraciones funcionales.
- 17. CARACTERÍSTICAS DEL HIPORBARISMO APLICACIONES EN LA MEDICINA • Presión a nivel del Mar = 760mmHg • Presión en Cuenca (2550 m.s.n.m) = 416,77 mmHg • Conforme disminuye la presión la presión parcial de oxigeno disminuye proporcionalmente, permaneciendo en todo momento ligeramente por debajo del 21% de la presión total conociendo la presión parcial del oxigeno al nivel del mar es de 159 mmHg. HIPOBARISMO HIPOXIA AMBIENTAL HIPOXIA FUNCIONAL LA PRESION Y LA PRESION PARCIAL DISMINUYEN, OCUPANDO MAYOR VOLUMEN LOS GASES EN EL CUERPO
- 18. APLICACIONES EN LA MEDICINA CARACTERÍSTICAS DIGESTIÓN LENTA (SENSACIÓN DE LLENURA) • El volumen de un gas es IP a su presión, entonces los gases producidos durante la digestión (6 L/día aproximado), adoptan mayores volúmenes a presiones menores. TAPADO DE OIDOS • 1. La tensión del tímpano se regula por una presión proveniente de la trompa de Eustaquio determinando a su vez por la temperatura corporal. • Otra representada por la presión atmosférica que incide en el conducto auditivo externo. (BOYLE) (GAY- LUSSAC)
- 19. EJERCICIOS
- 20. EJERCICIOS 1. El volumen de aire en los pulmones de una persona es de 615 ml aproximadamente, a una presión de 760 mmHg. La inhalación ocurre cuando la presión de los pulmones desciende a 752 mmHg. A qué volumen se expanden los pulmones?
- 21. EJERCICIOS 2. Un alpinista inhala 500 ml de aire a una temperatura de -10 ºC. Qué volumen ocupará el aire en sus pulmones si su temperatura corporal es de 37 ºC?
- 22. EJERCICIOS 3. Calcule la temperatura final de un gas que se encuentra en un recipiente cerrado, cuya presión cambio de 3 a 5 atmosferas si su tempera inicial fue de 24 ºC.
- 23. EJERCICIOS 4. Las llantas de un vehículo, deben estar a 20 ºC a una presión de 1,8 atm. Con el movimiento, se calientan hasta 50 ºC, pasando su volumen de 50 a 50,5 litros. Cual será la presión de la llanta tras la marcha?
- 24. EJERCICIOS 5. Un balón de 50 cc contiene cloro a la presión de 800 mmHg a 80ºC. La densidad del cloro es de 3,22 gr/L en concentración. ¿Cuál es el peso del cloro contenido?
- 25. EJERCICIOS 6. A partir del peso molecular, determinar la densidad del cloro a 0ºC y 760 mmHg.
