Cinetica quimica
•Descargar como PPTX, PDF•
0 recomendaciones•428 vistas
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Temperatura, presión, análisis dimensional e interpolación

Temperatura, presión, análisis dimensional e interpolación
Destacado
Practica 5 determinacion de estructuras cristalinas por difraccion de rayos x

Practica 5 determinacion de estructuras cristalinas por difraccion de rayos xJuan Andrés Castro Montoya
Destacado (20)
Facultad de ingenieria industrial jeymi ordoñez tema deformacion

Facultad de ingenieria industrial jeymi ordoñez tema deformacion
FUNDAMENTOS DE MATERIALES: COMPORTAMIENTO Y PROPIEDADES DE MANOFACTURA

FUNDAMENTOS DE MATERIALES: COMPORTAMIENTO Y PROPIEDADES DE MANOFACTURA
Desformacion y resistencia de los materiales aceros

Desformacion y resistencia de los materiales aceros
Practica 5 determinacion de estructuras cristalinas por difraccion de rayos x

Practica 5 determinacion de estructuras cristalinas por difraccion de rayos x
Similar a Cinetica quimica
Similar a Cinetica quimica (20)
Velocidad de las reacciones químicas y equilibrio químico

Velocidad de las reacciones químicas y equilibrio químico
Cinética enzimática sistema unireactivo enzimo 2015 (1).ppt

Cinética enzimática sistema unireactivo enzimo 2015 (1).ppt
Más de Jose Luis Tello Montero
Más de Jose Luis Tello Montero (6)
Cinetica quimica
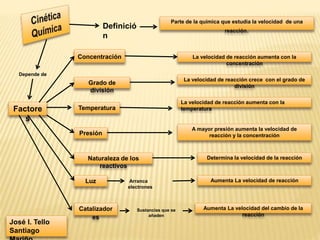
- 1. Naturaleza de los reactivos Presión TemperaturaFactore s Concentración Grado de división Parte de la química que estudia la velocidad de una reacción. Luz Catalizador es Determina la velocidad de la reacción A mayor presión aumenta la velocidad de reacción y la concentración La velocidad de reacción aumenta con la temperatura La velocidad de reacción crece con el grado de división La velocidad de reacción aumenta con la concentración Aumenta La velocidad de reacción Aumenta La velocidad del cambio de la reacción José l. Tello Santiago Arranca electrones Definició n Depende de Sustancias que se añaden
- 2. La velocidad de reacción de un sistema reactivo: a A + b B + ... → d D + e E + ... formulada en términos de concentraciones molares, se define como: v = − 1 /a d[A] /dt = − 1 /b d[B] /dt = ... = 1 /d d[D] /dt = 1 /e d[E]/ dt ≡ dξ/ dt donde ξe es el grado de avance de la reacción en términos de la concentración: ξe≡ ξ / V FORMULAS José l. Tello Santiago Si tenemos la siguiente reacción: A + B → C, se definen las velocidades media e instantánea como, Velocidad media: v = − ∆[A] /∆t = − ∆[B]/ ∆t = + ∆[C]/ ∆t Velocidad instantánea: v = − ∂[A]/ ∂t = − ∂[B] /∂t = + ∂[C] /∂t = k[A]m [B]n La velocidad, en general, varia con el transcurso de la reacción.
