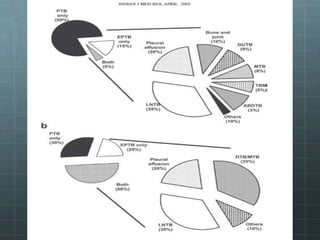
Este documento trata sobre la tuberculosis y el VIH/SIDA. Explica que la tuberculosis es una de las principales infecciones oportunistas que afectan a personas con VIH/SIDA debido a la debilidad del sistema inmunológico causada por el virus. Describe las manifestaciones clínicas, diagnóstico, tratamiento y patogénesis de la coinfección por tuberculosis y VIH, así como las interacciones entre los medicamentos antituberculosos y antirretrovirales.