Incrustar presentación
Descargar para leer sin conexión




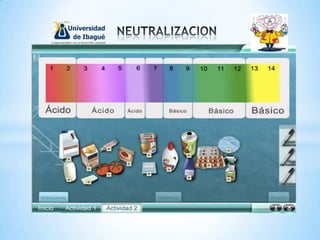
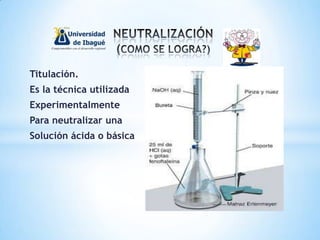

El documento resume las teorías históricas de los ácidos y bases según Lavoisier, Liebig, Arrhenius, Bronsted-Lowry y Lewis. También explica que la neutralización ocurre cuando un ácido y una base reaccionan en la misma cantidad de moléculas, y que la titulación es una técnica experimental para neutralizar soluciones ácidas o básicas.






