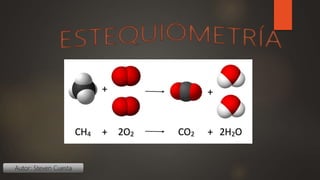
Estequiometria
- 2. Definición: Es el estudio de las relaciones cuantitativas que se producen entre los reactivos y los productos durante una reacción química. Estas relaciones pueden darse entre gramos, moles, partículas, etc. Cumple con la Ley de conservación de la materia
- 3. Ejemplos: 1. Determine cuantas moles de agua se producen en la oxidación de 2,5 moles de glucosa. 𝐶6 𝐻12 𝑂6 + 𝑂2 𝐻2O + C𝑂2 Siempre se debe verificar que la ecuación se encuentre balanceada 𝐶6 𝐻12 𝑂6 + 6 𝑂2 6 𝐻2O + 6 C𝑂2
- 4. = 1,5 moles 𝐻2O 𝐶6 𝐻12 𝑂6 + 6 𝑂2 6 𝐻2O + 6 C𝑂2 Procuramos partir del dato que conocemos, en este caso las 2,5 moles de glucosa 2,5 mol 𝐶6 𝐻12 𝑂6 6 mol 𝐻2O 1mol 𝐶6 𝐻12 𝑂6 Se concluye que a partir de 2,5 moles de glucosa se obtendrán 1,5 moles de agua
- 5. 2. Cuántos g de 𝐻2O se formarán a partir de 3 moles de 𝐻2 2 𝐻2 + 𝑂2 2 𝐻2O 3 mol 𝐻2 2 mol 𝐻2O 18g 𝐻2O 2mol 𝐻2 1mol 𝐻2O = 54 g 𝐻2O
- 6. 3. La sosa caustica (NaOH) se prepara comercialmente mediante la reacción entre el carbonato de sodio con la cal apagada Ca(OH)2. Cuántos gramos de NaOH se pueden obtener a partir de 1kg de carbonato de sodio 𝑁𝑎2 𝐶𝑂3 + 𝐶𝑎(𝑂𝐻)2 2 NaOH + 𝐶𝑎𝐶𝑂3 Como necesitamos encontrar g de NaOH, convertimos los kg de 𝑁𝑎2 𝐶𝑂3 a g. 1000g 𝑁𝑎2 𝐶𝑂3 1 mol 𝑁𝑎2 𝐶𝑂3 2 mol NaOH 40gNaOH 106g 𝑁𝑎2 𝐶𝑂3 1 mol 𝑁𝑎2 𝐶𝑂3 1 mol NaOH = 754,7g NaOH
- 7. 4. El amoniaco reacciona con el oxígeno para producir monóxido de nitrógeno y agua. a. Cuántos gramos de 𝐻2O se producen cuando reaccionan 85,15 g de amoniaco b. Cuántas moles de oxígeno se consumen c. Cuántas moléculas de monóxido de nitrógeno se producen. 4 𝑁𝐻3 + 5 𝑂2 4 NO + 6 𝐻2 𝑂 a. 85,15 g 𝑁𝐻3 1 mol 𝑁𝐻3 6 mol 𝐻2 𝑂 18 g 𝐻2 𝑂 17g 𝑁𝐻3 4 mol 𝑁𝐻3 1 mol 𝐻2 𝑂 = 135,23g 𝐻2 𝑂 b. 85,15 g 𝑁𝐻3 1 mol 𝑁𝐻3 5 mol 𝑂2 17g 𝑁𝐻3 4 mol 𝑁𝐻3 = 6,26 mol 𝑂2
- 8. Para realizar el literal c debemos recordar la constante del Número de Avogadro: 1mol = 6,022𝑥1023 átomos moléculas iones c. 85,15 g 𝑁𝐻3 1 mol 𝑁𝐻3 4 mol NO 6,022𝑥1023 moléculas NO 17g 𝑁𝐻3 4 mol 𝑁𝐻3 1 mol NO = 135,23g 𝐻2 𝑂
- 9. REFERENCIAS: Chang, R. (2010). Relaciones de masa en las reacciones químicas. En Químca (10ma edición ed., Vol. 1, pp. 78-85). McGraw-Hill Education. Chang, R. (2010). Relaciones de masa en las reacciones químicas. En Químca (10ma edición ed., Vol. 1, pp. 94-98). McGraw-Hill Education. Caballero Hurtado, Agustín (2006). Cómo resolver problemas de estequiometría. Editorial Filarias. p. 132. ISBN 978-84-932488-8-8