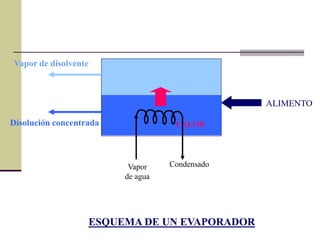
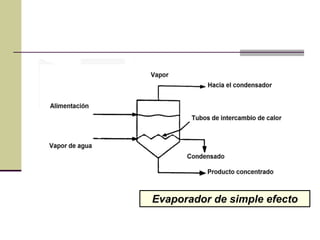
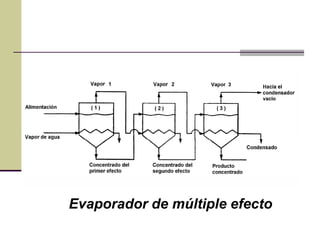
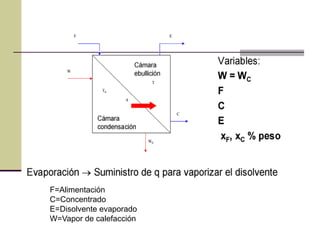
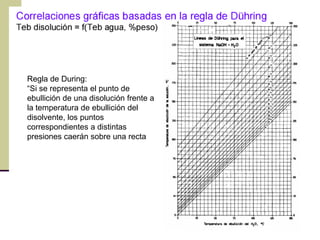
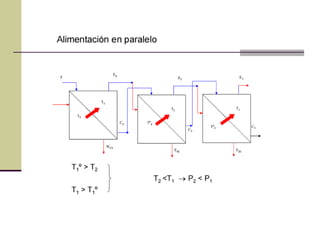
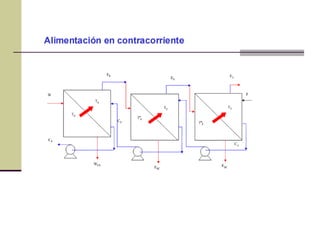
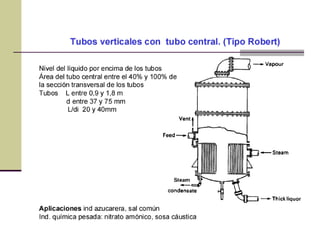
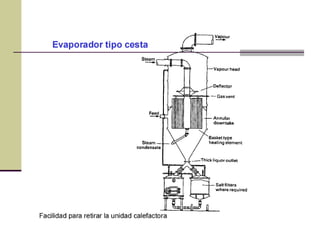
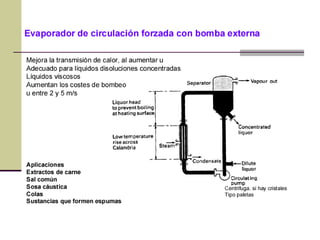
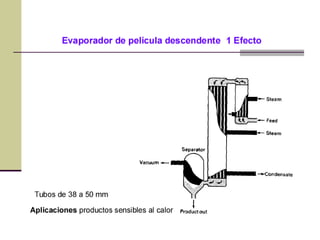
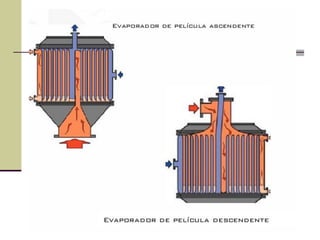
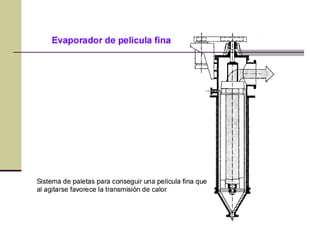
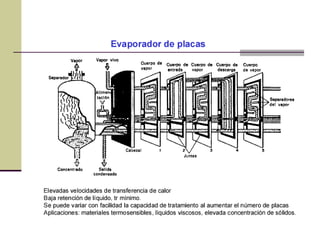
Este documento describe el proceso de evaporación para concentrar una solución mediante la eliminación del disolvente por ebullición. La evaporación consiste en hervir una solución de un soluto no volátil como NaOH y un disolvente volátil como el agua para separarlos. Un evaporador típicamente contiene un intercambiador de calor para hervir la solución y separar la fase vapor del líquido.