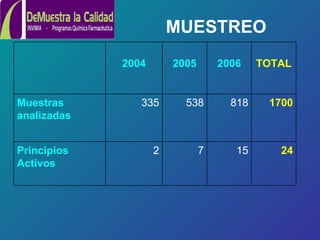
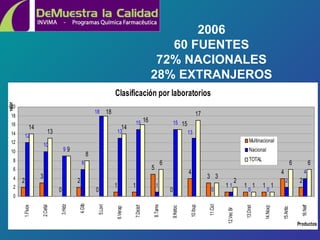
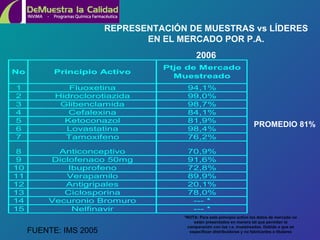
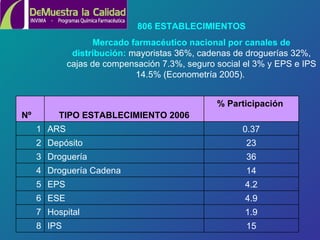
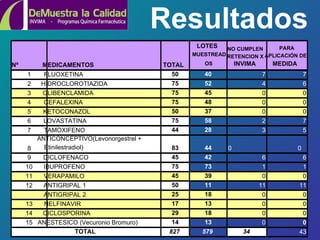
Este documento resume los resultados del programa "Demuestra la Calidad" del Instituto Nacional de Vigilancia de Medicamentos y Alimentos de Colombia entre 2004 y 2006. El programa analizó muestras de medicamentos en laboratorios universitarios y encontró una tasa de cumplimiento del 92.2% en 2005 y 95.9% en 2006. Algunos medicamentos como fluoxetina y antigripal mostraron incumplimientos relacionados posiblemente con problemas de fabricación. El programa busca expandir la red de laboratorios y ampliar la vigilancia a otros productos.