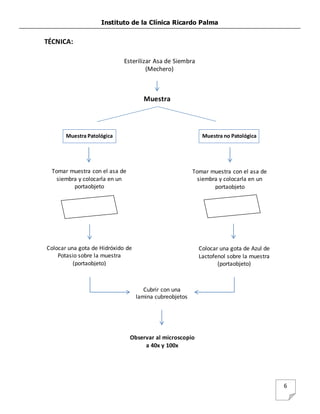
Este documento describe procedimientos para obtener y conservar muestras micóticas. Explica las diferencias entre levaduras y mohos, y los métodos para identificarlos. Detalla los pasos para preparar muestras patológicas y no patológicas usando hidróxido de potasio y azul de lactofenol respectivamente. Presenta resultados de muestras de tomate, queso y chicha identificando diferentes hongos. Concluye que estos reactivos permiten una observación clara facilitando el análisis de microorganism