Mapa conceptual quimica 1 power
•Descargar como PPTX, PDF•
0 recomendaciones•7,109 vistas
El documento describe los tipos principales de óxidos, incluidos los óxidos metálicos como el óxido de calcio utilizado en la fabricación de acero y cemento, y los óxidos no metálicos como el dióxido de carbono y el agua. También explica que la formación de enlaces químicos requiere energía y que los compuestos tienden a alcanzar una mayor estabilidad. Además, las propiedades de los elementos dependen del número de electrones en su último nivel.
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Enlace covalente

Contiene:
-Antecedente histórico del enlace covalente
-Conceptos y tipos de enlace covalente
-Las teorías del enlace covalente
Soluciones al ejercicio del cálculo del número de moles

Hace unos días publicamos algunos ejercicios para calcular el número de moles (http://www.slideshare.net/quimicaparatodosymas/ejercicios-calculo-del-numero-de-moles). Espero que hayais practicado un poco; aquí teneis las soluciones razonadas. Para más información http://quimicaparatodosymuchomas.blogspot.com.es/
Recomendados
Enlace covalente

Contiene:
-Antecedente histórico del enlace covalente
-Conceptos y tipos de enlace covalente
-Las teorías del enlace covalente
Soluciones al ejercicio del cálculo del número de moles

Hace unos días publicamos algunos ejercicios para calcular el número de moles (http://www.slideshare.net/quimicaparatodosymas/ejercicios-calculo-del-numero-de-moles). Espero que hayais practicado un poco; aquí teneis las soluciones razonadas. Para más información http://quimicaparatodosymuchomas.blogspot.com.es/
Propiedades periodicas

Propiedades Periódicas
Radio atómico
Radio Iónico
Energía de ionización
Electronegatividad
Afinidad Electronica
El Átomo - Configuración electrónica

Configuración electrónica del átomo, concepto de número másico, atómico, catión y anión
Química orgánica I - Lineales y Ramificados

Apuntes de formulación de química orgánica. Alcanos, alquenos, alquinos, etc...
Nomenclatura quimica

Con esta presentación podrán apreciar los tipos de nomenclatura química y algunos ejemplos prácticos.
Enlace Químico. Ejercicios. Enlace Iónico y Enlace Covalente

Ejercicos de Enlace Iónico y Enlace Covalente
Enlaces químicos 

¿Qué es un enlace?
Óxidos metálicos y no metálicos
Formación de enlaces interatómicos
Enlaces iónicos covalentes y puros
Representación de Lewis
Electronegatividad
Fuerzas Intermoleculares
Fuerzas dipolares
Puentes de hidrógeno
Fuerzas de London
DIFERENCIA EN LAS PROPIEDADES DE LOS COMPUESTOS
IÓNICOS Y COVALENTES
Más contenido relacionado
La actualidad más candente
Propiedades periodicas

Propiedades Periódicas
Radio atómico
Radio Iónico
Energía de ionización
Electronegatividad
Afinidad Electronica
El Átomo - Configuración electrónica

Configuración electrónica del átomo, concepto de número másico, atómico, catión y anión
Química orgánica I - Lineales y Ramificados

Apuntes de formulación de química orgánica. Alcanos, alquenos, alquinos, etc...
Nomenclatura quimica

Con esta presentación podrán apreciar los tipos de nomenclatura química y algunos ejemplos prácticos.
Enlace Químico. Ejercicios. Enlace Iónico y Enlace Covalente

Ejercicos de Enlace Iónico y Enlace Covalente
La actualidad más candente (20)
Enlace Químico. Ejercicios. Enlace Iónico y Enlace Covalente

Enlace Químico. Ejercicios. Enlace Iónico y Enlace Covalente
Similar a Mapa conceptual quimica 1 power
Enlaces químicos 

¿Qué es un enlace?
Óxidos metálicos y no metálicos
Formación de enlaces interatómicos
Enlaces iónicos covalentes y puros
Representación de Lewis
Electronegatividad
Fuerzas Intermoleculares
Fuerzas dipolares
Puentes de hidrógeno
Fuerzas de London
DIFERENCIA EN LAS PROPIEDADES DE LOS COMPUESTOS
IÓNICOS Y COVALENTES
Enlaces quimicos por Estefania López.

enlaces quimicos union ofuerzas que se dan entre atomos, iones, moleculas porsu nivel deelectronegatividad se da tambien tipos deenlaces detallados a continuacion.
Enlaces Atómicos (QM08 - PDV 2013)

Especialidad: Química Mención
Guía 08: Enlaces Atómicos
Material: Exclusivo Pre-Universitario Pedro de Valdivia
Año: 2013
Enlaces químicos

Describe como se forman los diferentes enlaces químicos, estructuras de lewis entre muchos aspectos importantes.
Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...

Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...schizophrenia_candy_blue
Enlaces químicos y estructura de lewis

Todas las sustancias que forman los objetos que constituyen el patrimonio cultural están constituidos por átomos que se unen en moléculas las cuales son las bases estructurales de toda la materia. Los químicos han ideado modelos que expliquen la forman en cómo estos átomos se unen para formar moléculas y éstas como forman la materia que vemos y conocemos. Uno de estos modelos es el de Lewis.
Similar a Mapa conceptual quimica 1 power (20)
Mapa Menta Lectrua #1 ¿En que difieren los óxidos metálicos de los óxidos no ...

Mapa Menta Lectrua #1 ¿En que difieren los óxidos metálicos de los óxidos no ...
Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...

Mapa mental de lectura #1 "En que difieren los óxidos metálicos de los no met...
Más de IsaiAlex
Más de IsaiAlex (16)
Ejercicios de estructuras de lewis isai alejandro lozano cristobal

Ejercicios de estructuras de lewis isai alejandro lozano cristobal
Ejercicios de estructuras de lewis isai alejandro lozano cristobal

Ejercicios de estructuras de lewis isai alejandro lozano cristobal
Mapa conceptual quimica 1 power
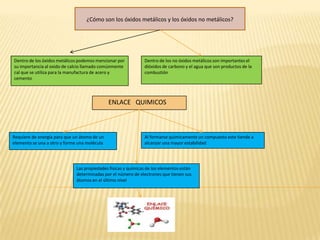
- 1. ¿Cómo son los óxidos metálicos y los óxidos no metálicos? Dentro de los óxidos metálicos podemos mencionar por su importancia al oxido de calcio llamado comúnmente cal que se utiliza para la manufactura de acero y cemento Dentro de los no óxidos metálicos son importantes el dióxidos de carbono y el agua que son productos de la combustión ENLACE QUIMICOS Requiere de energía para que un átomo de un elemento se una a otro y forme una molécula Al formarse químicamente un compuesto este tiende a alcanzar una mayor estabilidad Las propiedades físicas y químicas de los elementos están determinadas por el número de electrones que tienen sus átomos en el último nivel
- 2. ¿Porque se forma un enlace? De acuerdo con el número atómico de los elementos, los electrones se distribuyen en diferentes niveles de energía Al establecer la distribución electrónica de los elementos se ah encontrado que para el caso de los gases nobles, con excepción del helio tienen 8 electrones en su último nivel Regla del Octeto Los átomos que participan en las reacciones químicas tienden a adoptar la configuración electrónica propia de un gas noble Tienen 8 electrones en su último nivel, lo cual le confiere estabilidad a sus átomos La regla del octeto se puede cumplir cuando existe una trasferencia de electrones de un átomo a otro
- 3. Diagrama de Lewis Es la representación de los electrones en el último nivel de un átomo por medio de puntos, pequeños círculos o cruces, con la finalidad de visualizar lo que ocurre con estos electrones al formarse el enlace químico Cabe destacar que los electrones del último nivel de un átomo son los responsables del comportamiento químico