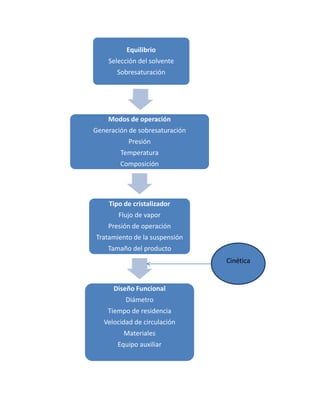
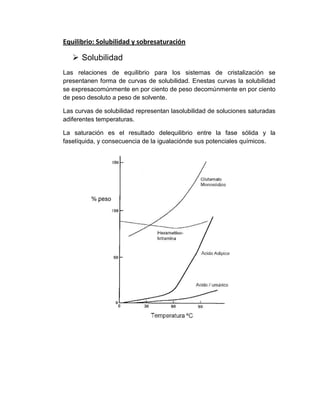
La cristalización es una técnica para obtener sólidos cristalinos mediante la disminución de la solubilidad de una sustancia en una disolución saturada, lo que puede lograrse por enfriamiento o evaporación. Esto permite purificar sustancias o separar mezclas. El diseño de cristalizadores requiere considerar el equilibrio y la cinética del proceso para controlar el tamaño y forma de los cristales obtenidos.