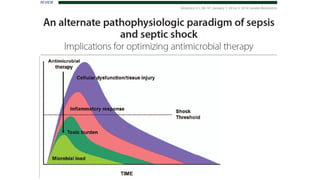
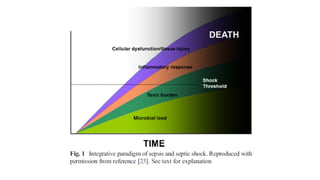
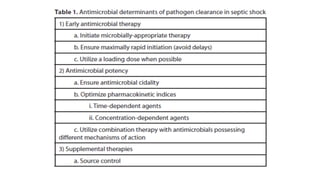
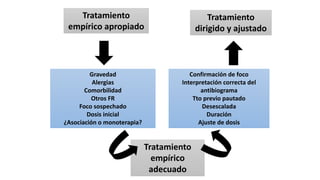
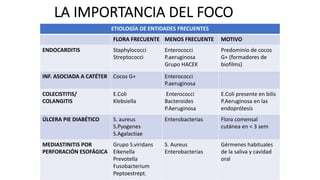
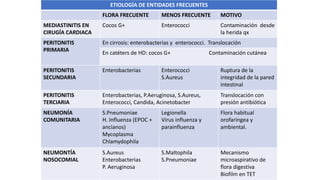
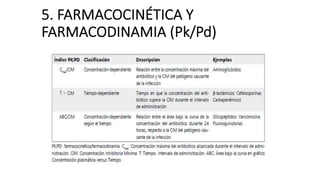
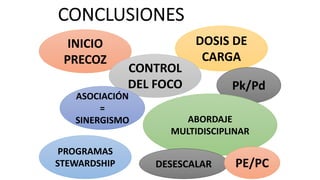
Este documento trata sobre la optimización de la antibioterapia. Resalta la importancia de (1) iniciar el tratamiento empírico de forma precoz para cubrir los microorganismos más probables, (2) considerar la gravedad del paciente y el foco de infección al elegir los antibióticos, y (3) ajustar las dosis y duración del tratamiento según los resultados microbiológicos para una mejora clínica.