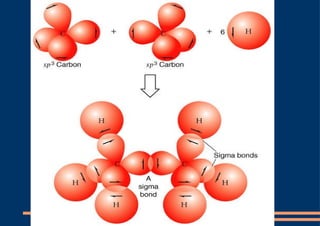
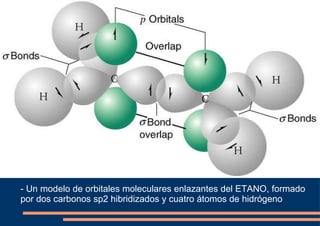
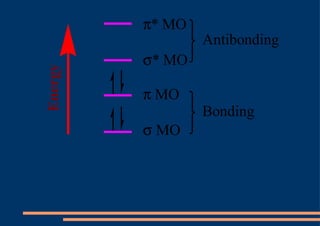
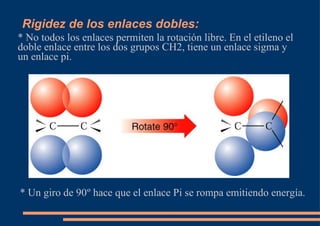
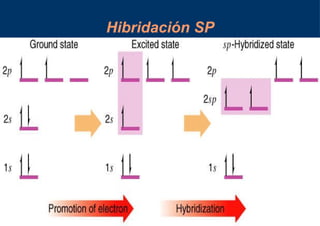
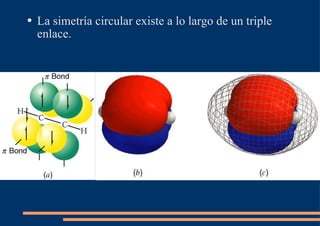
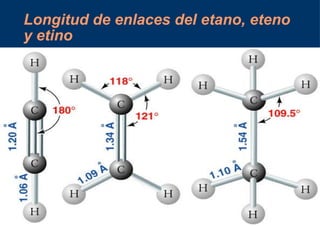
El documento describe los diferentes tipos de orbitales atómicos y orbitales moleculares, así como los conceptos de hibridación sp3, sp2 y sp. La hibridación sp3 da como resultado orbitales híbridos orientados a 109.5° que forman la estructura tetraédrica del metano. La hibridación sp2 forma orbitales en un triángulo que dan la estructura planar del eteno, con un enlace pi formado por los orbitales p. La hibridación sp da como resultado orbitales en línea recta que forman el triple enlace lineal en el