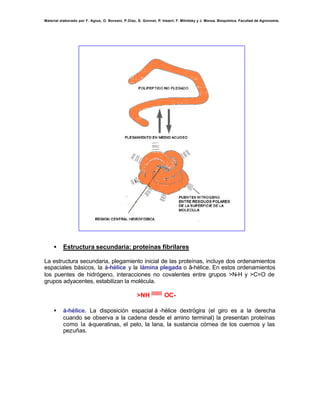
El documento resume las características fundamentales de los péptidos y proteínas. Se explica que están compuestos por aminoácidos unidos mediante enlaces peptídicos, y que su función biológica depende de la secuencia específica de aminoácidos. Las proteínas son macromoléculas que adquieren una estructura tridimensional determinada por su secuencia primaria a través de fuerzas como puentes de hidrógeno e interacciones hidrofóbicas. Algunas proteínas están formadas por subunidades que