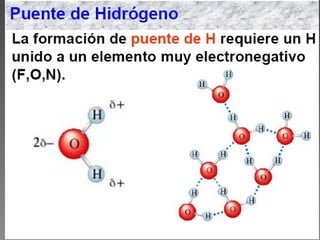
Puente de h
- 2. El puente de hidrógeno se describe frecuentemente como una interacción electrostática, dipolo-dipolo. Sin embargo, tiene algunas características de enlace covalente: •es direccional, •relativamente intenso, •produce distancias interatómicas más cortas que la suma de los radios de van der Waals •comúnmente incluye a un número limitado de vecinos, lo que se puede interpretar como una especie de valencia. Estas características covalentes son más significativas cuando están involucrados átomos de elementos muy electronegativos. El carácter parcialmente covalente de los puentes de hidrógeno genera las siguientes preguntas: •¿A qué molécula o átomo pertenece el núcleo de hidrógeno? •¿Qué átomo debería ser rotulado como donador y cuál como aceptor? Esta pregunta se puede responder fácilmente basados en las distancias interatómicas en el sistema X-H---Y; la distancia X-H es aproximadamente igual a 1.1 Å, mientras que la distancia H---Y está entre 1.6 a 2.0 Å. Los líquidos que presentan puentes de hidrógeno se les conoce como líquidos asociados.
- 3. Los puentes de hidrógeno pueden variar en intensidad desde muy débiles (1-2 kJ mol−1) a extremadamente fuertes (40 kJ mol−1), como ocurre en el ion HF2−. Valores típicos incluyen: O—H...:N (29 kJ/mol ó 6.9 kcal/mol) O—H...:O (21 kJ/mol ó 5.0 kcal/mol) N—H...:N (13 kJ/mol ó 3.1 kcal/mol) N—H...:O (8 kJ/mol ó 1.9 kcal/mol) HO—H...:OH3+ (18 kJ/mol* ó 4.3 kcal/mol) *Datos obtenidos a partir de cálculos de dinámica molecular. Structure and energetics of the hydronium hydration shells Omer Markovitch and Noam Agmon J. Phys. Chem. A; 2007; 111(12) pp 2253 – 2256.
