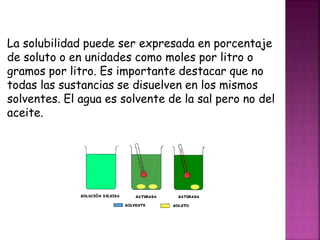
La solubilidad es la capacidad de una sustancia (soluto) para disolverse en otra (solvente), formando una solución homogénea. La solubilidad depende de factores como la naturaleza química del soluto y solvente, la temperatura y la presión. Algunas sustancias como el agua son solventes universales, mientras que otras como los aceites no se disuelven en agua. Los solventes suelen ser líquidos volátiles y tóxicos que pueden formar mezclas inflamables. La cristalización es un pro