Incrustar presentación
Descargar para leer sin conexión
![Calcular el pH de 25.0 ml de HCl 0.100 M. Solución: El HCl es un electrolito fuerte, es decir, completamente disociado en H+ y Cl-, por lo que esta disolución es 0.100 M en H+. pH= -log [H+] pH= -log [0.100] pH= 1.00](https://image.slidesharecdn.com/titulacin-valoracin1-090818210405-phpapp02/85/TitulacioN-ValoracioN1-2-320.jpg)
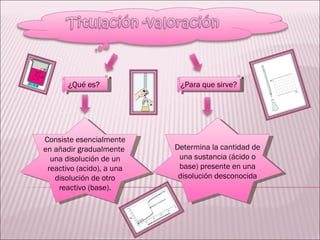
El documento describe una titulación ácido-base, un método para determinar la concentración de un ácido o base desconocida añadiendo gradualmente una disolución del otro reactivo opuesto hasta alcanzar el punto de equivalencia. Proporciona un ejemplo de cálculo del pH de una solución de HCl usando su concentración de iones hidrógeno.

![Calcular el pH de 25.0 ml de HCl 0.100 M. Solución: El HCl es un electrolito fuerte, es decir, completamente disociado en H+ y Cl-, por lo que esta disolución es 0.100 M en H+. pH= -log [H+] pH= -log [0.100] pH= 1.00](https://image.slidesharecdn.com/titulacin-valoracin1-090818210405-phpapp02/85/TitulacioN-ValoracioN1-2-320.jpg)