Ley de los gases ideales
•
0 recomendaciones•87 vistas
MAPAS DE GASES MAPAS DE GASES MAPAS DE GASES
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Actividad Integradora. Una Ley de los Gases. Módulo 12

Actividad Integradora. Una Ley de los Gases. Módulo 12
Principios de quimica y estructura ena2 - ejercicio 12 volumen ocupado por...

Principios de quimica y estructura ena2 - ejercicio 12 volumen ocupado por...
Actividad Integradora. Ley General de los Gases. Módulo 12

Actividad Integradora. Ley General de los Gases. Módulo 12
Principios de quimica y estructura ena2 - ejercicio 06 cambio de la densid...

Principios de quimica y estructura ena2 - ejercicio 06 cambio de la densid...
Cervantes canto lilianaelena_m12s3_leygeneraldegases

Cervantes canto lilianaelena_m12s3_leygeneraldegases
Similar a Ley de los gases ideales
Similar a Ley de los gases ideales (20)
SEMANA N° 10 Quimica General - Mg. MIGUEL VASQUEZ HUAMAN.pdf

SEMANA N° 10 Quimica General - Mg. MIGUEL VASQUEZ HUAMAN.pdf
67786760 ejercicios-resueltos-de-gases-ideales-y-gases-reales-roldan

67786760 ejercicios-resueltos-de-gases-ideales-y-gases-reales-roldan
67786760 ejercicios-resueltos-de-gases-ideales-y-gases-reales-roldan

67786760 ejercicios-resueltos-de-gases-ideales-y-gases-reales-roldan
Más de AlejandroGarcia985
Más de AlejandroGarcia985 (20)
Geodesia Geodesia Geodesia Geodesia Geodesia Geodesia 

Geodesia Geodesia Geodesia Geodesia Geodesia Geodesia
Último
Último (20)
Introducción:Los objetivos de Desarrollo Sostenible

Introducción:Los objetivos de Desarrollo Sostenible
MAYO 1 PROYECTO día de la madre el amor más grande

MAYO 1 PROYECTO día de la madre el amor más grande
RETO MES DE ABRIL .............................docx

RETO MES DE ABRIL .............................docx
TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx

TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx
ACUERDO MINISTERIAL 078-ORGANISMOS ESCOLARES..pptx

ACUERDO MINISTERIAL 078-ORGANISMOS ESCOLARES..pptx
Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf
DE LAS OLIMPIADAS GRIEGAS A LAS DEL MUNDO MODERNO.ppt

DE LAS OLIMPIADAS GRIEGAS A LAS DEL MUNDO MODERNO.ppt
Clasificaciones, modalidades y tendencias de investigación educativa.

Clasificaciones, modalidades y tendencias de investigación educativa.
Caja de herramientas de inteligencia artificial para la academia y la investi...

Caja de herramientas de inteligencia artificial para la academia y la investi...
Ley de los gases ideales
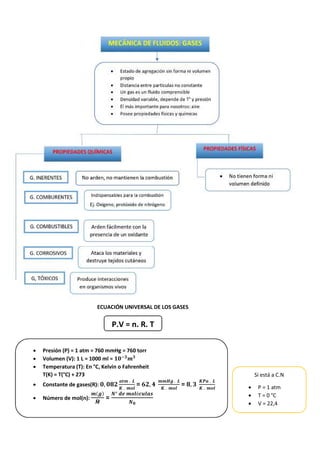
- 1. ECUACIÓN UNIVERSAL DE LOS GASES Presión (P) = 1 atm = 760 mmHg = 760 torr Volumen (V): 1 L = 1000 ml = Temperatura (T): En °C, Kelvin o Fahrenheit T(K) = T(°C) + 273 Constante de gases(R): , . . = , . . = , . . Número de mol(n): = ° é ! P.V = n. R. T Si está a C.N P = 1 atm T = 0 °C V = 22,4
- 2. EJERCICIO1: Un gas ocupa un volumen de 2 l en condiciones normales. ¿Qué volumen ocupará esa misma masa de gas a 2 atm y 50ºC? Solución Como partimos de un estado inicial de presión, volumen y temperatura, para llegar a un estado final en el que queremos conocer el volumen, podemos utilizar la ley combinada de los gases ideales, pues la masa permanece constante: ; . 1 1 1 0 T V P T V P o o la temperatura obligatoriamente debe ponerse en K l V K atm K l atm V K V atm K l atm 18 , 1 ; 273 . 2 373 . 2 . 1 ; 323 . 2 273 2 . 1 1 1 1 Como se observa al aumentar la presión el volumen ha disminuido, pero no de forma proporcional, como predijo Boyle; esto se debe a la variación de la temperatura. ECUACIÓN GENERAL DE LOS GASES LEY DE BOYLE - MARIOTTE LEY DE CHARLES LEY DE GAY - LUSSAC "#$# = "&$& Proceso isotérmico T constante V IP P $# '# = $& '& Proceso isobórico P constante V DP T $# '# = $& '& Proceso isométrico V constante P DP T "#$# '# = "&$& '& Proceso isomásico Masa constante
- 3. EJERCICIO 2: Se tiene un volumen de 40 cm^3 de oxígeno a una presión de 380 mm de Hg. ¿Qué volumen ocupará a una presión de 760 mm de Hg? Si la temperatura es constante. Solución. Aplicando la ley General de gases. P1V1 P2V2 P1V1 = P2V2 = T1 T2 Datos. P1 = 380mmHg P1V1 P2 = V2 V1 = 40cm^3 (380mmHg)(40cm^3) = V2 P2 = 760mmHg 760mmHg V2 =? 20cm^3 = V2
- 4. Se deduce lo siguiente, si la presión es menor mayor es el volumen o si la presión es mayor menor es el volumen.