Tabla periódica
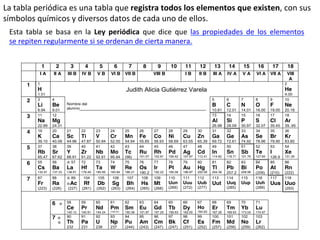
- 1. 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 I A II A III B IV B V B VI B VII B VIII B I B II B III A IV A V A VI A VII A VIII A 1 1 H 1.01 Judith Alicia Gutiérrez Varela 2 He 4.00 2 3 Li 6.94 4 Be 9.01 Nombre del alumno__________________________________________________________ 5 B 10.81 6 C 12.01 7 N 14.01 8 O 16.00 9 F 19.00 10 Ne 20.18 3 11 Na 22.99 12 Mg 24.31 13 Al 26.98 14 Si 28.09 15 P 30.97 16 S 32.07 17 Cl 35.45 18 Ar 39..95 4 19 K 39.10 20 Ca 40.08 21 Sc 44.96 22 Ti 47.87 23 V 50.94 24 Cr 52.00 25 Mn 54.94 26 Fe 55.85 27 Co 58.93 28 Ni 58.69 29 Cu 63.55 30 Zn 65.39 31 Ga 69.72 32 Ge 72.61 33 As 74.92 34 Se 78.96 35 Br 79.90 36 Kr 83.80 5 37 Rb 85.47 38 Sr 87.62 39 Y 88.91 40 Zr 91.22 41 Nb 92.91 42 Mo 95.94 43 Tc (98) 44 Ru 101.07 45 Rh 102.91 46 Pd 106.42 47 Ag 107.87 48 Cd 112.41 49 In 114.82 50 Sn 118.71 51 Sb 121.76 52 Te 127.60 53 I 126.9 54 Xe 131.29 6 55 Cs 132.91 56 Ba 137.33 57 La 138.91 72 Hf 178.49 73 Ta 180.95 74 W 183.84 75 Re 186.21 76 Os 190.2 77 Ir 192.22 78 Pt 195.08 79 Au 196.97 80 Hg 200.59 81 Tl 204.38 82 Pb 207.2 83 Bi 208.98 84 Po (209) 85 At (210) 86 Rn (222) 7 87 Fr (223) 88 Ra (226) 89 Ac (227) 104 Rf (261) 105 Db (262) 106 Sg (263) 107 Bh (264) 108 Hs (265) 109 Mt (268) 110 Uun (269) 111 Uuu (272) 112 Uub (277) 113 Uut 114 Uuq (285) 115 Uup 116 Uuh (289) 117 Uus 118 Uuo (293) 6 58 Ce 140.12 59 Pr 140.91 60 Nd 144.24 61 Pm (144.91) 62 Sm 150.36 63 Eu 151.97 64 Gd 157.25 65 Tb 158.93 66 Dy 162.50 67 Ho 164.93 68 Er 167.26 69 Tm 168.93 70 Yb 173.04 71 Lu 174.97 7 90 Th 232 91 Pa 231 92 U 238 93 Np 237 94 Pu (244) 95 Am (243) 96 Cm (247) 97 Bk (247) 98 Cf (251) 99 Es (252) 100 Fm (257) 101 Md (258) 102 No (259) 103 Lr (262) La tabla periódica es una tabla que registra todos los elementos que existen, con sus símbolos químicos y diversos datos de cada uno de ellos. Esta tabla se basa en la Ley periódica que dice que las propiedades de los elementos se repiten regularmente si se ordenan de cierta manera.
- 4. Propiedades de los metales 1. Forman redes cristalinas metálicas, en las cuales los ca<ones se hallan perfectamente ordenados en el espacio. Los empaquetamientos que presentan, esencialmente, son 3: Estructura cúbica centrada en las caras Estructura cúbica centrada en el cuerpo Estructura hexagonal Aunque se trate de empaquetamientos compactos, mo<vo por el cual los metales suelen presentar dureza, el empaquetamiento cúbico centrado en el cuerpo es el menos compacto de los tres. Esto hace que los metales que lo presentan sean más blandos compara<vamente que los otros metales, por ejemplo, el sodio y el li<o son tan blandos que se pueden cortar con un cuchillo.
- 5. 2. Presentan una elevada densidad (masa por unidad de volumen) debido, precisamente, al empaquetamiento metálico de los ca<ones. 3. Elevadas conducAvidades térmica y eléctrica, debido a la gran movilidad de los electrones de valencia, que hemos visto ya en el modelo del gas de electrones y también en la teoría de bandas. 4. Gran deformabilidad, porque las capas de ca<ones se pueden desplazar entre sí sin alterar la estructura. Por ello se pueden es<rar en hilos, como el cobre (propiedad que recibe el nombre de ducAlidad) y también en láminas, como el aluminio (maleabilidad). 5. En general, altos puntos de fusión y ebullición, lo cual implica que hace falta una gran can<dad de energía para separar los átomos que forman el reIculo cristalino. No obstante, sus puntos de fusión varían notablemente dentro de un intervalo muy amplio: el mercurio es líquido a temperatura ambiente, el galio funde a 29ºC y el wolframio a 3380ºC. 6. Brillo metálico. La mayoría de los metales pulidos no absorbe ninguna radiación luminosa incidente, sino que la refleja en su totalidad. De ahí que los vemos brillar con un brillo plateado en su mayoría. 7. Emisión de electrones. Ya vimos en la explicación del efecto fotoeléctrico que los metales pueden emi<r electrones al ser irradiados con una radiación de la frecuencia adecuada. Del mismo modo, esto también puede suceder por calor, lo que recibe el nombre de efecto termoiónico.
- 7. Propiedades de los no metales Son malos conductores del calor. Son malos conductores de la electricidad. La mayoría son gaseosos a temperatura ambiente. No presentan brillo (lustre). Tienen densidad baja. Tienen puntos de ebullición y de fusión bajos. No son maleables. No son dúc<les. Sus átomos <enden a ganar electrones convir<éndose en aniones (-‐). H
- 8. Metaloides Tienen propiedades intermedias entre metales y no metales, por lo que <enen algunas aplicaciones especiales. Por ejemplo, los metaloides silicio y germanio se u<lizan en la construcción de los componentes electrónicos de las computadoras.
- 9. Familias de elementos Químicos Las familias son agrupaciones de elementos que <enen propiedades similares.
- 10. LAS FAMILIAS SON: Alcalinos: Los metales alcalinos están situados en el grupo 1 de la tabla periódica y no se encuentran libres en la naturaleza debido a su gran ac<vidad química. Todos ellos <enen un solo electrón en su úl<ma capa que ceden con facilidad para formar enlace iónico con otros elementos. Los metales alcalinos son Li, Na, K, Rb, Cs y Fr, siendo los dos úl<mos los más reac<vos del grupo. Como la mayoría de los metales, son dúc<les, maleables, y buenos conductores del calor y la electricidad. Los metales alcalinos reaccionan violentamente con el agua, ardiendo en ella, por lo que deben ser manejados con cuidado.
- 11. Alcalinotérreos: Los metales alcalino-‐térreos, Be, Mg, Ca, Sr, Ba y Ra se encuentran situados en el segundo grupo del sistema periódico. Todo ellos <enen 2 electrones en su úl<ma capa lo que les confiere una gran reac<vidad. No se encuentran libres en la naturaleza sino formando compuestos de <po iónico, a excepción de los del berilio que presentan un importante porcentaje covalente. Al contrario que los alcalinos, muchas de las sales de los metales alcalino-‐térreos son insolubles en agua.
- 12. Lantánidos: Los lantánidos, también llamados primeras <erras raras están situados en el 6º período y grupo 3. La mayor parte de estos elementos han sido creados ar<ficialmente, es decir NO EXISTEN EN LA NATURALEZA. Esta familia está compuesta por los siguientes elementos: La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb
- 13. Ac1nidos: Conocidos también como segundas <erras raras, todos ellos están situados en el grupo 3 del sistema periódico y en el 7º período. La mayor parte de estos elementos han sido creados ar<ficialmente, es decir NO EXISTEN EN LA NATURALEZA. Pertenecen a esta familia: Ac, Th, Pa, U, Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No
- 14. Metales de transición: Situados entre los grupos 3 y 12, se caracterizan porque sus electrones de valencia proceden de más de una capa y presentan las propiedades Ipicas de los metales: buena conducción del calor y la electricidad, duc<lidad, maleabilidad y brillo metálico. Par<cularmente importantes son el hierro, el cobalto y el níquel, únicos elementos capaces de producir un campo magné<co. Esta familia está formada por: Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Y, Zr, Nb, Mo, Tc, Ru, Rh, Pd, Ag, Cd,Lu, Hf, Ta, W, Re, Os, Ir, Pt, Au, Hg,Lr, Rf, Db, Sg, Bh, Hs, Mt
- 15. Otros metales: Los elementos clasificados como otros metales se encuentran repar<dos entre los grupos 13, 14 y 15. Su carácter metálico es menos acentuado que el de los elementos de transición, no suelen presentar estados de oxidación variables y sus electrones de valencia sólo se encuentran en su capa externa. Forman parte de este grupo de elementos: Al, Ga, In, Tl, Sn, Pb, Bi
- 16. Metaloides o semimetales : Son los elementos que separan los metales de transición de los no metales y son conocidos también como metaloides por tener propiedades intermedias entre metales y no metales. Algunos de ellos, como el silicio y el germanio, son semiconductores y por ello se usan en la industria de los ordenadores. Otros elementos de esta familia son: boro, arsénico, an<monio, telurio, polonio.
- 17. No metales: Los no metales se caracterizan por ser malos conductores del calor y la electricidad y no pueden ser es<rados en hilos o láminas. A la temperatura ambiente algunos son gases (como el oxígeno) y otros sólidos (como el carbono). Los sólidos no <enen brillo metálico. El carbono da lugar a un gran número de compuestos cuyo estudio recibe el nombre de química orgánica. H
- 18. Halógenos: Los halógenos se encuentran situados en el grupo 17 cons<tuido por los elementos no metálicos flúor, cloro, bromo, yodo y astato. Son elementos bastante reac<vos porque por su estructura electrónica final <enden a estabilizarse completando el octeto final para lo cual capturan un electrón o lo comparten dando lugar así a compuestos iónicos o covalentes respec<vamente. Estos formadores de sales (Significado de la palabra halógenos) <enen como principal estado de oxidación el -‐1 y se presentan en los tres estados a temperatura ambiente: Sólido: I y At Líquido: Br Gaseoso: F y Cl
- 19. Gases nobles: Los gases nobles están situados en el grupo 18 de la tabla periódica: helio, neón, argón, criptón, xenón y radón. Todos ellos <enen 8 electrones en su úl<ma capa (a excepción del helio que completa su única capa con 2 electrones) y debido a ello son prác<camente inertes. Sólo a par<r de la segunda mitad del siglo XX se han producido algunos compuestos de gases nobles.
