Ca gástrico .pptx
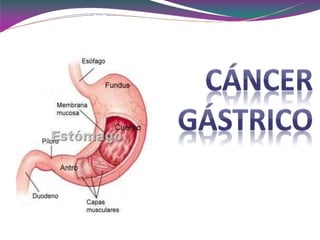
- 2. ANATOMÍ A • Estómago: 5 partes •Según el origen de la neoplasia: síntomas y consecuencias diferentes. •También afecta al tto.: unión gastro-esofágica y cardias Tto. como cáncer de estómago. •6 grupos linfáticos perigástricos: Temprana invasión linfática en50%. • Órganos cercanos al estómago: el colon,el hígado, el bazo, el intestino delgado y el páncreas. HÍGADO
- 3. La pared del estómago tiene cinco capas. La capa más profunda es la mucosa: producción HCl y enzimas digestivos. Origen de la mayoría de los cánceres de estómago. Bajo ésta una capa de apoyo llamada submucosa, cubierta por la muscularis, una capa de músculo que mueve y mezcla el contenido delestómago. Las dos capas externas: subserosa y serosa, actúan como capas que envuelven al estómago. ANATOMÍ A Fondo Esófago Antro Píloro
- 4. Uno de los cánceres más comunes en el mundo, aunque disminuyendo en Occidente. Neoplasia Maligna que se origina en el epitelio gástrico y que progresivamente invade o compromete las diferentes capas de la paredgástrica. El tipo histólogico más frecuente: 96% es el Adenocarcinoma; el 4% restante: Linfomas, Tumores Carcinoides, Sarcoma departes blandas (GIST). DEFINICIÓN Y TIPOS ADENOCARCINOMA GÁSTRICO
- 5. • DIFUSO - Incidencia creciente - No localizado - Estómago proximal - Tendencia metástasis - Peor pronóstico • INTESTINAL - Incidencia decreciente - Localizado - Estómago distal - H.Pylori - Mejor pronóstico Adenocarcinoma: Clasif. Histo Lauren
- 6. FACTORES DE RIESGO Sexo masculino. Edad avanzada. Habitantes de Japón, Islandia, Chile, Colombia, CostaRica. Dietas con alto contenido de sal y alimentos ahumados. Nitrosaminas. Consumo decigarrillos. Bajo nivel socio económico ( distal) Helicobacter pylori. mineros, expuestos a asbesto y a serrín Gastritis crónicaatrófica. Metaplasia intestinal. Factores genéticos (IL-IB, IFNGR1, MTHF ) Síndrome de Peutz-Jeghers Gastrectomía Anemia perniciosa
- 8. CÁNCER GÁSTRICO HEREDITARIO Representa 1%de todoslos casos. Mutación germinal en gen E caderina (CDH1) enun 30 % aproximadamente. Tipo difuso. HELICOBACTER PYLORI LAMAYORÍADE LOS PACIENTES CON H.PYLORI NO DESARROLLAN CÁNCER GÁSTRICO !!!! Alta incidencia de H. Pylori en gastritis: papel en iniciar la lesión de la mucosa y desarrollo de gastritis atrófica crónica. Tipo intestinal.
- 9. Se estiman 988000 casos nuevos en 2008 (7,8% total). Cuarto cáncer más común en el mundo: Pulmón>Mama>Colon-recto>Gástrico. (Sexto en España) > 70% en países desarrollados; 50% en Asia (China). 2ª causa de muerte por cáncer en el mundo (ambos sexos). 736000 muertes (9,7% total). (Quinta en España). EPIDEMIOLO GÍA
- 10. : Es más frecuente en hombres que en mujeres, 2:1 : La Incidencia aumenta con la edad a partir de la cuarta década, haciéndose máxima en la séptima. En nuestro medio la edad media al diagnóstico está en torno a los 60 años. similar a Mortalidad. La ha disminuido en los últimos 15años: la Incidencia ha disminuido pues la Supervivencia apenas ha mejorado. malo (diagnóstico tardío): a los 5 años 20-25%. EPIDEMIOLO GÍA
- 14. Cáncer GástricoAvanzado Pérdida de peso 92% Dolor abdominal 74% Anorexia 60% Náuseas yVómitos 46% Plenitud epigástrica 35% Masa epigástricapalpable 30% Hemorragia digestiva 20% Disfagia 20% Metástasis 10% Asintomática 2% SIGNOS Y SÍNTOMAS Cáncer Inicial • Asintomático • Anemia • Dispepsia 50%
- 15. Anamnesis y examen físico con valoración del peso y estado nutricional Permormance status( PS) Hemograma. Coagulación. Bioquímica. Marcadores CEAy CA 19.9 ECG Esofagogastroscopia Biopsia gástrica endoscópica TACtoracoabdominal y pélvico Ecoendoscópia. uTNM ¿ laparoscopia? ¿ gammagrafía ósea? DIAGNÓSTI CO
- 16. TRATAMIEN TO Tratamiento endoscópico: resección de mucosa (EMR) Cirugía: Gastrectomía Linfadenectomía Tratamiento multimodal: - Neoadyuvante - Adyuvante Tratamiento paliativo
- 18. CIRUGÍA: CONSECUENCIAS Nutr. Hosp. (2002) 17 (5) 236-239
- 20. QT NEOADYUVANTE (peri- operatoria) En pacientes con cáncer gástrico operable o adenocarcinoma de esófago bajo disminuye eltamaño del tumor y el estadio y mejora significativamente TLP y SG. Estándar en Europa
- 22. QT NEOADYUVANTE (peri- operatoria) PFS(meses): 17vs24. OS(meses):20 vs24. Disminución riesgo muerte 25%
- 24. QT-RT ADYUVANTE (QT-RT post- operatoria) La RT loco-regional + 5FU/LV mejora significativamente la SG y SLE en pacientes con cáncer gástrico operado. Estándar en EE.UU
- 25. QT-RT ADYUVANTE (QT-RT post- operatoria) PFS(meses): 19vs 30. OS(meses):27 vs36. Disminución riesgo muerte: 24%
- 26. QT ADYUVANTE
- 27. QT ADYUVANTE
- 28. YUVAN TE Se considera adicional al tratamiento potencialmente curativo (cirugía) cuando: No existe enfermedad a distancia INDICACIONES: PS < 2. 5FU 425 mg / m2 d Q ía x T5 A díaD s + LEUCOVORÍN 20 mg / m2 día x 5 días EnX fe1 rmC I C edL O admacroscópica resecada RT (45 Gy) 5 F MU á4 r0 g0 enm eg s/nme2gativos LEUCOVORÍN 10 mg / m2 4 primeros días y 3 últimos 5FU 4 2 5 Edm ag d/ <m 702 ad ñí a osx .5 días Adecu+ada función renal, hepática LEUCOVORÍyNm2e0dmulgar/.m2 día x 5 días EsX ta2 dC ioI C sL I O I -S IV .(M0) T3-4, N+ (no hacer en T2)
- 29. QT PALIATIVA
- 30. QT PALIATIVA Wagner AD, Grothe W, Behl S, Kleber G, Grothey A, Haerting J, Fleig WE. Chemotherapy for advanced gastric cancer. The Cochrane Database of Systematic Reviews: Reviews 2005 Issue 2 John Wiley &Sons, Ltd Chichester,UK DOI: 10.1002/14651858.CD004064.pub2
- 31. QT PALIATIVA 5 PREGUNTAS >50 1. Mejor terapia de apoyo vs quimioterapia 2. Monoagente vscombinación 13estudios (1522pacientes) 3. Combinaciones Con Fluoruracilo Sin Fluoruracilo 35 estudios (4274 pacientes) 4. FU/DDP/Antraciclinas vsFU/DDP 5. FU/Antraciclinas/DDP vs sinDDP 10estudios (1648 pacientes)
- 32. 1. Quimioterapia vs mejor terapia de apoyo Número de estudios Número de pacientes MTA (meses) QT (meses) OS 3 184 4.3 11 TTP 2 144 2-2.7 6.5-7.8 WagnerAD, Grothe W, Behl S, Kleber G, GrotheyA, Haerting J, Fleig WE. Chemotherapy for advanced gastric cancer. The Cochrane Database of Systematic Reviews: Reviews 2005 Issue 2 John Wiley & Sons, Ltd Chichester, UK DOI: 10.1002/14651858.CD004064.pub2
- 33. 2. Monoagentevs combinación Número de estudios Número de pacientes MonoQT (meses) PoliQT (meses) OS 10 1338 5.9 7.0 WagnerAD, Grothe W, Behl S, Kleber G, GrotheyA, Haerting J, Fleig WE. Chemotherapy for advanced gastric cancer. The Cochrane Database of Systematic Reviews: Reviews 2005 Issue 2 John Wiley & Sons, Ltd Chichester, UK DOI: 10.1002/14651858.CD004064.pub2
- 34. Reference Drug, dose Regimen 3. Combinación CON/SIN 5FU Cycle duration, days 21 days ECF Findlay, M; 1994 Epirubicin: 50 mg/m2 d1 Cisplatin: 60 mg/m2 d1 5 FU: 200mg/m2/day continuous infusion ECX Cunningham, D; 2008 (REAL-2) Epirubicin: 50 mg/m2 d1 21 days Cisplatin: 60 mg/m2 d1 Capecitabine:625 mg/m2 twice daily EOX Cunningham, D; 2008 (REAL-2) Epirubicin: 50 mg/m2 d1 21 days Oxaliplatin 130 mg/m2 d1 Capecitabine: 625 mg/m2 twice daily DCF Van Cutsem, E; 2006 Docetaxel 75 mg/ m2 d1 21 days Cisplatin 75 mg/m2 d1 5-FU: 750mg/m2/day continuous infusion, d1-d5 Cisplatin/ irinotecan Ajani, J; 2002 Cisplatin: 30 mg/m2 weekly � Irinotecan: 65 mg/m2 weekly for 4 of every 6 weeks FOLFIRI Bouche, O; 2004 LV 200mg/m2 over 2 hr d1, d2 14 days 5 FU: 400 mg/m2 bolus d1, d2 then 600/m2 over 22 hours d1, d2 Irinotecan: 180 mg/m2 d1
- 35. 4. 5-FU/cisplatino/antraciclina versus 5- FU/cisplatino (Sin antraciclinas) WagnerAD, Grothe W, Behl S, Kleber G, GrotheyA, Haerting J, Fleig WE. Chemotherapy for advanced gastric cancer. The Cochrane Database of Systematic Reviews: Reviews 2005 Issue 2 John Wiley & Sons, Ltd Chichester, UK DOI: 10.1002/14651858.CD004064.pub2
- 36. 5 - 5-FU/cisplatino/antraciclina versus5- FU/antraciclina (Sincisplatino)
- 37. DOCETAXEL Phase III TAX325 superiority study (TCF vs CF) OXALIPLATIN Phase III REAL-2 non-inferiority study (EOF vsEOX vs ECF vs ECX) Phase III superiority study (FLO vs FLC) ORALFLUOROPYRIMIDINES (S-1, capecitabine) Phase III non-inferiority study (CX vs CF) IRINOTECAN Phase IIIV306 non-inferiority study (IF vs CF) PACLITAXEL Phase II GEMCITABINE Phase II TARGETED BIOLOGICAL THERAPIES (eg bevacizumab, cetuximab) Pre-clinical to PhaseII AGENTES ACTIVOS
- 38. QT PALIATIVA CONCLUSIONES 1.La quimioterapia es mejor que la mejor terapia de apoyo. 2. Los poliagentes son mejores que los monoagentes. 3.El fluoruracilo puede ser remplazado por otro agente, pero se incrementa la toxicidad en forma sustancial, por lo que se recomienda que sea incluido. 4. Los tripletes con antraciclinas, cisplatino y fluoruracilo son mejores que los dupletes con un beneficio de magnitud pequeña pero real con un incremento en la toxicidad a más agentes sean utilizados.
- 39. REAL-2 TRIAL
- 40. REAL-2 TRIAL
- 41. To-Ga TRIAL 5-FU/Xeloda+CsP 5-FU/Xeloda+CsP + Trastuzumab p SG 11.1meses 13.8 meses 0.0048 SLP 5.5 meses 6.7 0.0002
- 42. TRATAMIEN TO
- 43. A) TRATAMIENTO PERIOPERATORIO (MAGIC): -ECOG 0-1. -Adenocarcinoma gástrico, de unión gastroesofágica o de tercio inferior esofágico. -Estadio ≥ II. Pacientes resecables al diagnóstico. -Buena función hepática, renal, cardiaca y medular. -Pacientes sin sangrado digestivo activo ni obstrucción gástrica ADENOCARCINOMA GÁSTRICO RESECABLE ECF: o Epirrubicina: 50 mg/m2 día 1 o Cisplatino: 60 mg / m2 día 1cada 3 semanas o Fluoracilo 200 mg / m2 /día en IC
- 44. CASO CLÍNICO Varón de 62 años que acudió a urgencias por astenia de dos semanas de evolución. Se le detecta anemia microcítica y deriva al S. Digestivo. Se realiza EDA que informa que a nivel del antro hay una gran masa ulcerada sin llegar a estenosar la luz. La biopsia es compatible con adenocacinoma. Otras: Ecoendoscopia confirmatoria. Varias adenopatías. Serología: CEAYCA19.9normales. 8/11/11: Derivado a S. Oncología. Juicio Clinico y radiológico: uT3N1Mo: (Estadio IIb). QT NEOADYUVANTE con ECF
- 45. CASO CLÍNICO 25/1/12: Se realiza una Ecoendoscopia tras tres ciclos de QT: uT2N1Mo. Se programa cirugía. 10/2/12: Es intervenido mediante Gastrectomía total. Valoración: Adenocarcinoma tipo intestinal, bien diferenciado que infiltra submucosa sin alcanzar muscularis(pT1). Libres de tumor las 16adenopatías (pN0): pT1N0M0.(Estadio IA). 1/3/12: Se reinica tresciclos QT. 27/5/12: Finaliza QT e inicia revisiones. Actualmente: Continúa con revisones cada tres meses.
- 46. ADENOCARCINOMA GÁSTRICO RESECABLE B) TRATAMIENTOADYUVANTE O POSTOPERATORIO (McDonald): - ECOG < 2. - Adecuada función renal, hepática y medular. - Estadios: pT3-T4 y/o pN+. - Edad menor o igual a 70 años. - 5 ciclos de 5FU-LV (1 ciclo cada 28 días): 1ºciclo: 5FU 425 mg/m2/d e Isovorin 10mg/m2/d x5días. 2ª ciclo (4 primeros días de la RT): 5FU 400 mg/m2/d e Isovorin 10mg/m2/d x 4días. 3ª ciclo (3 últimos días de la RT): 5FU 400 mg/m2/d e Isovorin 10 mg/m2/d x3días. 4º ciclo: 5FU 425 mg/m2/d e Isovorin 10mg/m2/d x 5días. 5º ciclo: 5FU 425 mg/m2/d e Isovorin 10mg/m2/d x 5días. - RT:45 Gy en 25 fracciones (5 semanas).
- 47. CASO CLÍNICO Paciente de 56 años remitida a C. Digestivo de modo urgente por el médico de cabecera por epigastralgia y hemorragia digestiva realizándose EDA. Hallazgos: En subcardias zona de mucosa con biopsia + para adenocarcinoma. 30/06/09: Intervenida mediante gastrectomía, omenectomía y esofagoyeyunostomía en Y de Roux. Adenocarcinoma pobremente diferenciado tipo difuso que infiltra pared llegando a serosa (pT3), y metástasis en 6 de las 18 adenopatías aisladas (pN2) y bordes (-). pT3N2M0: (Estadio IIIa). 30/07/09: En C.Oncología inicia esquema McDonald con 5 ciclos de 5FU-LV + RT que finaliza en 12/09. Comienza revisiones.
- 48. CASO CLÍNICO 14/01/10: Se observa en TC una lesión de mal definida de unos 2 cm en el segmento IV del hígado no presente en TC anteriores. JC: Progreso de CA Gástrico a nivel hepático. PLAN: Inico QT 2ªlínea con DCX cada 21 días pues ECOG 2. Finaliza en 5/10. 10/06/10: Laparotomía con lobectomía izquierda. JC: Enfermedad venoclusiva, no se advierte lesión tumoral. Actualmente: Continúa en seguimiento, sospecha clínica de enfermedad pero sin evidencia de la misma en pruebas de imagen y MT normales.
- 49. ADENOCARCINOMA GÁSTRICO METASTÁSICO A) En pacientes con ECOG < 2 y adecuada función renal, hepática, cardiaca y medular: ECXx 6-8 ciclos. B) En pacientes con insuficiencia renal, o contraindicación de sobrecarga hídrica: EOX x 6-8 ciclos. Epirrubicina: 50 mg/m2 día1 Oxaliplatino: 130mg / m2 día 1 Capecitabina 625 mg / m2 /12 horas continuo. C) En pacientes HER-2 neu positivos, valorar: Herceptin 8 mg/kg seguido de 6 mg/kg d1 Cisplatino 80 mg/m2 d1 Capecitabina 1000 mg/m2/12 h d1-14 ó Fluoracilo 800 mg/m2 IC dias 1-5. D) En pacientes con edad avanzada, ECOG > 2, valorar: Capecitabina 1000-1250 mg / m2 /12 h d1-14 cada 3 semanas . cada 3semanas cada 3semanas
- 50. ADENOCARCINOMA GÁSTRICO METASTÁSICO 2ª LINEA: Tratamiento individualizado en pacientes con buen estado general. Entre otros: FOLFIRI DOCETAXEL-CISPLATINO cada 3semanas: - Docetaxel 75 - 85 mg/m2 dia 1. - Cisplatino 75 mg/m2 dia1. IRINOTECAN 300 - 350 mg/m2 cada3 semanas. CAPECITABINA 1250 mg/m2/ 12 horas durante 14 dias cada 21 dias
- 51. CONCLUSIO NES Estadios < II: Cirugía Tumores operados estadio≥2: QT+RT en esquema McDonald Tumores localmente avanzados y operables estadio (Estadio II-III ) : QT neoadyuvante con esquema MAGIC. Tumores metastásicos (Estadio IV): QTpaliativa