Disoluciones químicas 2m
•Descargar como PPTX, PDF•
3 recomendaciones•1,814 vistas
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Recomendados
Guía de apoyo n°3 q2 m 2013 disoluciones químicas y propiedades coligativas

Guía de apoyo n°3 q2 m 2013 disoluciones químicas y propiedades coligativasLaboratoriodeciencias Altazor
Más contenido relacionado
La actualidad más candente
La actualidad más candente (19)
Destacado
Guía de apoyo n°3 q2 m 2013 disoluciones químicas y propiedades coligativas

Guía de apoyo n°3 q2 m 2013 disoluciones químicas y propiedades coligativasLaboratoriodeciencias Altazor
Destacado (16)
Guía de apoyo n°3 q2 m 2013 disoluciones químicas y propiedades coligativas

Guía de apoyo n°3 q2 m 2013 disoluciones químicas y propiedades coligativas
Similar a Disoluciones químicas 2m
Similar a Disoluciones químicas 2m (20)
SOLUCIONES en la vida diaria para ayudar a combatir las enfermedades

SOLUCIONES en la vida diaria para ayudar a combatir las enfermedades
Soluciones, equilibrios iónicos y enlaces químicos acuosos

Soluciones, equilibrios iónicos y enlaces químicos acuosos
Más de sanmarinocollege
Más de sanmarinocollege (20)
Último
Último (20)
Movimientos Precursores de La Independencia en Venezuela

Movimientos Precursores de La Independencia en Venezuela
LA ECUACIÓN DEL NÚMERO PI EN LOS JUEGOS OLÍMPICOS DE PARÍS. Por JAVIER SOLIS ...

LA ECUACIÓN DEL NÚMERO PI EN LOS JUEGOS OLÍMPICOS DE PARÍS. Por JAVIER SOLIS ...
Introducción:Los objetivos de Desarrollo Sostenible

Introducción:Los objetivos de Desarrollo Sostenible
PPT GESTIÓN ESCOLAR 2024 Comités y Compromisos.pptx

PPT GESTIÓN ESCOLAR 2024 Comités y Compromisos.pptx
la unidad de s sesion edussssssssssssssscacio fisca

la unidad de s sesion edussssssssssssssscacio fisca
Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
LINEAMIENTOS INICIO DEL AÑO LECTIVO 2024-2025.pptx

LINEAMIENTOS INICIO DEL AÑO LECTIVO 2024-2025.pptx
6° SEM30 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx

6° SEM30 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx
Disoluciones químicas 2m
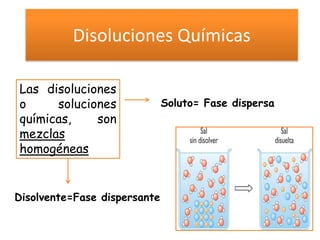
- 1. Disoluciones Químicas Las disoluciones o soluciones Soluto= Fase dispersa químicas, son mezclas homogéneas Disolvente=Fase dispersante
- 2. Conceptos Claves • Soluto: Sustancia que se disuelve en un disolvente para formar una disolución. • Disolvente: Sustancia que está presente en mayor cantidad en una disolución
- 3. Proceso de disolución • 1) Se produce la separación de las partículas de disolvente. • 2) Las partículas del soluto comienzan a disociarse dentro del disolvente • 3) Finalmente, las moléculas del disolvente y del soluto se mezclan, formando la disolución. Ver pág. 18
- 4. Tipos de disoluciones 3 Criterios para la clasificación: Estado físico de sus componentes Proporción de los componentes Conductividad eléctrica
- 5. Estado físico de los componentes
- 6. Proporción de los componentes Según la cantidad de soluto se clasifican: • Disoluciones insaturadas: En estas, hay muy poca cantidad de soluto, el disolvente puede seguir admitiendo más soluto.
- 7. • Disoluciones Saturadas o concentradas Son aquellas que a una temperatura determinada no pueden seguir admitiendo más soluto. Si la temperatura aumenta, la capacidad para admitir más soluto aumenta.
- 8. • Disoluciones sobresaturadas La cantidad de soluto sobrepasa la capacidad de disolvente para disolver a una temperatura dada.
- 9. Conductibilidad electrónica • Aquellas sustancias ( soluto) que en disolución acuosa son CONDUCTORES de electricidad se denominan Electrolitos y sus disoluciones Disoluciones electrolíticas.
- 10. • Un electrolito: es una sustancia que se disocia inmediatamente en medio acuoso en particulas con cargas eléctricas IONES
- 11. Teoría de la disociación electrolítica • Svante Arrehenius: “ Que ciertas sustancias, frente al contacto con el agua, forman iones positivos y negativos que conducen corriente electrica”.