15. BIODISPONIBILIDAD Y BIOEQUIVALENCIA_PARTE 3.pdf
•
0 recomendaciones•10 vistas
El documento describe los pasos clave en el diseño de un ensayo clínico, incluyendo la descripción del producto a investigar, los criterios de inclusión y exclusión de voluntarios, el análisis farmacocinético, la evaluación de seguridad y tolerancia, y las consideraciones éticas. Además, explica los posibles factores que pueden dar lugar a diferencias entre los ensayos de formulaciones, como el efecto de secuencia, período y formulación. Por último, resume los aspectos clave de un ensayo in vitro de disoluc
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Fundamentos teoricos de Biodisponibilidad

Biodisponibilidad.
Fundamentos teoricos de los estudios de biodisponibilidad
Evaluación de farmacos

Las pruebas en animales sobre el potencial de fármacos nuevos pueden abreviarse en el caso de algunos fármacos, como los anticancerígenos y medicamentos contra el SIDA.
Farmacologia Clinica Y Farmacovigilancia AñO 2011

Este documento contiene definiciones relacionadas con la farmacología clínica y los ensayos clínicos. Define términos como investigador, sujeto del estudio, producto en investigación, protocolo, eficacia y toxicidad. También describe las diferentes fases del desarrollo de un nuevo fármaco, incluidos los estudios preclínicos y las cuatro fases de los ensayos clínicos en humanos.
Farmacología Clínica y Farmacovigilancia - Año 2012

Este documento presenta definiciones clave relacionadas con la farmacología clínica y la farmacovigilancia. Explica las diferentes fases de investigación clínica de nuevos fármacos, incluidas las fases preclínicas, las fases 1 a 3 con ensayos en humanos, y la fase de farmacovigilancia posterior a la comercialización. También describe los estudios de toxicidad necesarios antes de los ensayos clínicos y los requisitos éticos para la investigación en humanos.
Gestion de Calidad 2013 10-1 buenas practicas clinicas

Este documento presenta información sobre las buenas prácticas clínicas. Explica las diferentes etapas del desarrollo de un medicamento, incluyendo las fases clínicas y la producción a escala. También describe las resoluciones y guías que rigen las buenas prácticas clínicas, como la Resolución 1490/2007 del Ministerio de Salud de Argentina. El documento proporciona detalles sobre los procesos de escalado, fabricación, estudios de estabilidad y producción de lotes para ensayos clínicos.
Buenaspracticasclinicas quilmes 2013

Este documento presenta información sobre las buenas prácticas clínicas. Explica las diferentes etapas del desarrollo de un medicamento, incluyendo las fases clínicas y la producción a escala. También describe las resoluciones y guías que rigen las buenas prácticas clínicas, como la Resolución 1490/2007 del Ministerio de Salud de Argentina. El documento proporciona detalles sobre los procesos de escalado, fabricación, estudios de estabilidad y producción de lotes para ensayos clínicos.
Desarrollo de los medicamentos

El documento describe el proceso de desarrollo de medicamentos, incluyendo investigación preclínica en animales, 4 fases de ensayos clínicos en humanos para evaluar seguridad y eficacia, y monitoreo posteriores a la comercialización. El proceso toma años y cuesta millones de dólares, pero ha llevado al descubrimiento de tratamientos que salvan vidas.
El ensayo clinico

El documento describe las cuatro fases de los ensayos clínicos. La Fase I evalúa la seguridad en un pequeño grupo de sujetos sanos. La Fase II evalúa la eficacia y dosis en pacientes. La Fase III evalúa la eficacia y seguridad en grandes grupos. La Fase IV monitorea la seguridad a largo plazo una vez que el producto es comercializado. Cada fase proporciona información para avanzar el desarrollo y la aprobación del producto.
Recomendados
Fundamentos teoricos de Biodisponibilidad

Biodisponibilidad.
Fundamentos teoricos de los estudios de biodisponibilidad
Evaluación de farmacos

Las pruebas en animales sobre el potencial de fármacos nuevos pueden abreviarse en el caso de algunos fármacos, como los anticancerígenos y medicamentos contra el SIDA.
Farmacologia Clinica Y Farmacovigilancia AñO 2011

Este documento contiene definiciones relacionadas con la farmacología clínica y los ensayos clínicos. Define términos como investigador, sujeto del estudio, producto en investigación, protocolo, eficacia y toxicidad. También describe las diferentes fases del desarrollo de un nuevo fármaco, incluidos los estudios preclínicos y las cuatro fases de los ensayos clínicos en humanos.
Farmacología Clínica y Farmacovigilancia - Año 2012

Este documento presenta definiciones clave relacionadas con la farmacología clínica y la farmacovigilancia. Explica las diferentes fases de investigación clínica de nuevos fármacos, incluidas las fases preclínicas, las fases 1 a 3 con ensayos en humanos, y la fase de farmacovigilancia posterior a la comercialización. También describe los estudios de toxicidad necesarios antes de los ensayos clínicos y los requisitos éticos para la investigación en humanos.
Gestion de Calidad 2013 10-1 buenas practicas clinicas

Este documento presenta información sobre las buenas prácticas clínicas. Explica las diferentes etapas del desarrollo de un medicamento, incluyendo las fases clínicas y la producción a escala. También describe las resoluciones y guías que rigen las buenas prácticas clínicas, como la Resolución 1490/2007 del Ministerio de Salud de Argentina. El documento proporciona detalles sobre los procesos de escalado, fabricación, estudios de estabilidad y producción de lotes para ensayos clínicos.
Buenaspracticasclinicas quilmes 2013

Este documento presenta información sobre las buenas prácticas clínicas. Explica las diferentes etapas del desarrollo de un medicamento, incluyendo las fases clínicas y la producción a escala. También describe las resoluciones y guías que rigen las buenas prácticas clínicas, como la Resolución 1490/2007 del Ministerio de Salud de Argentina. El documento proporciona detalles sobre los procesos de escalado, fabricación, estudios de estabilidad y producción de lotes para ensayos clínicos.
Desarrollo de los medicamentos

El documento describe el proceso de desarrollo de medicamentos, incluyendo investigación preclínica en animales, 4 fases de ensayos clínicos en humanos para evaluar seguridad y eficacia, y monitoreo posteriores a la comercialización. El proceso toma años y cuesta millones de dólares, pero ha llevado al descubrimiento de tratamientos que salvan vidas.
El ensayo clinico

El documento describe las cuatro fases de los ensayos clínicos. La Fase I evalúa la seguridad en un pequeño grupo de sujetos sanos. La Fase II evalúa la eficacia y dosis en pacientes. La Fase III evalúa la eficacia y seguridad en grandes grupos. La Fase IV monitorea la seguridad a largo plazo una vez que el producto es comercializado. Cada fase proporciona información para avanzar el desarrollo y la aprobación del producto.
Módulo 2 - Farmacovigilancia

Módulo 2 - FarmacovigilanciaCIPPS - Facultad de Medicina de la Universidad Nacional Autónoma de México
El documento trata sobre epidemiología, farmacovigilancia y farmacoepidemiología. En 3 oraciones resume que la epidemiología estudia la distribución y determinantes de la salud y enfermedades en poblaciones humanas, la farmacovigilancia recopila y monitorea información sobre efectos adversos de medicamentos para prevenir daño a pacientes, y la farmacoepidemiología aplica métodos epidemiológicos para integrar información sobre el uso y efectos de fármacos en condiciones reales de práctica clínica.001 Investigacion clinica en farmacologia

El documento proporciona una introducción a los estudios de investigación en farmacología clínica. Explica que estos estudios sistemáticos se realizan en humanos para descubrir los efectos y reacciones de los ingredientes farmacéuticos activos. Detalla las cuatro fases de los estudios clínicos para el desarrollo de nuevos medicamentos, así como los criterios para la participación de voluntarios y el proceso de aprobación regulatoria. En resumen, brinda una visión general del propósito y metodología de los estudios de
Ensayo clinico

Este documento describe los diferentes tipos de estudios clínicos, incluyendo ensayos clínicos. Explica que los ensayos clínicos son estudios experimentales prospectivos que evalúan la eficacia de intervenciones médicas mediante la manipulación intencional de variables y la asignación aleatoria de participantes a grupos. También describe las diferentes fases de los ensayos clínicos y los elementos clave como la aleatorización, enmascaramiento y análisis de datos.
Clinical trials

Este documento proporciona una introducción a los ensayos clínicos. Explica que los ensayos clínicos implican la aplicación de un tratamiento experimental a personas para observar sus efectos. Describe los diferentes tipos de diseños de ensayos clínicos como paralelos y cruzados. También cubre temas como la aleatorización, enmascaramiento, análisis de datos, monitoreo de seguridad, representatividad y generalización de resultados. El objetivo final es evaluar la seguridad y eficacia de nuevos tratam
Farmaepidyvigil

Este documento define la farmacoepidemiología como el estudio de la distribución de los determinantes de la salud y las enfermedades en las poblaciones humanas con respecto al uso y efectos de los fármacos. Describe diferentes tipos de estudios de farmacoepidemiología como estudios de consumo cualitativos y cuantitativos, y estudios de oferta de medicamentos como auditorías terapéuticas. También explica conceptos clave de farmacovigilancia como las clasificaciones de las reacciones adversas a medicamentos y los métodos para evaluar la
Procesos de industrialización de fármacos

Este documento describe el proceso de industrialización de fármacos, incluyendo las etapas de investigación y desarrollo, pre-formulación, pre-clínica, formulación, evaluación, registro y uso. Explica cada etapa del proceso de elaboración de medicamentos, desde la investigación de moléculas hasta los ensayos clínicos y la comercialización. También analiza los efectos adversos de los medicamentos y el mercado farmacéutico mundial.
Glosario

Este documento presenta definiciones de varios términos relacionados con la farmacología y la investigación clínica. Algunos de los términos definidos incluyen absorción, aclaramiento, acontecimiento adverso, adyuvante, aleatorización, alternativas terapéuticas, bioequivalencia, bioética, buenas prácticas clínicas, buenas prácticas de fabricación, buenas prácticas de farmacovigilancia, buenas prácticas de laboratorio, calidad de vida y calidad de
Ensayo clinico controlado modificado

Este documento describe los ensayos clínicos controlados y sus elementos clave. Explica los diferentes tipos de diseños de ensayos como los aleatorizados, los de control concurrente y los históricos. También describe los pasos en la selección de participantes, los tipos de estudios controlados como los abiertos, de simple y doble ciego, y los factores que afectan la interpretación de los resultados.
Desarrollo del medicamento

El documento describe las diversas etapas en el desarrollo de un medicamento, incluyendo estudios preclínicos en animales, 4 fases de ensayos clínicos en humanos para probar seguridad y eficacia, y monitoreo posteriores a la aprobación para detectar efectos adversos inesperados.
Metodo medicina cientifica (1)

Este documento describe tres tipos de investigación clínica y sus características. La investigación clínica se puede clasificar en (1) investigación para aumentar el conocimiento sobre la eficacia y seguridad de un producto, (2) investigación sobre las causas o mecanismos de una enfermedad, y (3) investigación para satisfacer las necesidades de tratamiento de pacientes que han agotado otras opciones. El documento también discute diferentes diseños de estudios clínicos como aleatorizados, controlados, ciegos y otros factores a considerar en la investig
Proceso de desarrollo de fármacos

El proceso de desarrollo de fármacos involucra varias etapas complejas que pueden tomar más de una década. Inicialmente, los científicos diseñan el fármaco conceptualmente identificando un objetivo y estrategia. Luego producen pequeñas cantidades para pruebas preclínicas en animales. Finalmente, realizan tres fases de estudios clínicos en humanos para probar seguridad, dosificación y eficacia a escalas crecientes antes de que las agencias regulatorias autoricen su distribución global,
Ensayos clinicos fase i, ii y iii

Los ensayos clínicos de fase III evalúan la eficacia y seguridad de un tratamiento experimental en una amplia muestra de pacientes representativa, comparándolo con otros tratamientos disponibles de manera controlada, aleatorizada y preferiblemente ciega para reproducir las condiciones de uso habituales y determinar el balance beneficio-riesgo.
ENSAYO CLÍNICO EXPO ANDRES.docx

El documento describe diferentes tipos de ensayos clínicos, incluyendo ensayos unicéntricos versus multicéntricos, ensayos controlados versus no controlados, y diferentes técnicas de enmascaramiento como ensayos simples, dobles o triples ciegos. Explica que los ensayos multicéntricos y controlados son más robustos, mientras que los ensayos no controlados y unicéntricos son más susceptibles a sesgos.
Estudios experimentales en epidemiología

Este documento describe los estudios experimentales en epidemiología. Explica que en este tipo de estudios, el investigador manipula la exposición de un grupo para compararlo con otro grupo no expuesto. Luego describe tres tipos de estudios experimentales: ensayos de campo, que estudian factores preventivos en sujetos sanos; ensayos clínicos, que evalúan tratamientos en pacientes; y ensayos comunitarios, que incluyen intervenciones a nivel comunitario. Finalmente, detalla los pasos para la ejecución de estudios experimentales y sus ventaj
Diseño de un estudio aleatorizado con enmascaramiento

Este documento describe los aspectos clave del diseño de un estudio aleatorizado con enmascaramiento. Explica la importancia de la asignación aleatoria y el enmascaramiento para minimizar la influencia de variables de confusión. Luego, se centra en la elección de las condiciones de intervención y testigo, las variables de respuesta, los efectos adversos, y los criterios de selección de participantes. Finalmente, discute la medición de variables basales, la aleatorización, y el enmascaramiento en el estudio.
Ensayo clinicofase12

Este documento describe las distintas fases de los ensayos clínicos, enfocándose en las fases I y II. Explica que la fase I evalúa la seguridad y tolerabilidad de un nuevo fármaco en un pequeño número de voluntarios sanos, así como su farmacocinética y dosis máxima tolerada. La fase II explora preliminarmente la eficacia y relación dosis-respuesta. Ambas fases ayudan a orientar los estudios posteriores antes de probar el fármaco en pacientes.
Desarrollo y regulación de fármacos

El documento describe los métodos de investigación y desarrollo de nuevos fármacos y su regulación. Explica que los nuevos fármacos se originan en investigaciones públicas y luego son desarrollados por la industria farmacéutica a un alto costo. Detalla las etapas de descubrimiento de fármacos, evaluación preclínica en animales, ensayos clínicos en humanos y aprobación regulatoria considerando factores como seguridad, eficacia y factores de confusión. Finalmente, aborda los retos en el
Taller de iniciación a la investigación clínica. Parte I

Este documento describe diferentes tipos de estudios clínicos, incluyendo estudios descriptivos transversales y longitudinales, estudios analíticos observacionales como estudios de cohortes y casos y controles, y ensayos clínicos. Explica conceptos clave como la clasificación, finalidad, secuenciación temporal, control de asignación a factores de estudio, e inicio del estudio en relación a la cronología de los hechos. Resalta la importancia de considerar factores como la ética, población de estudio, aleatorización, intervención,
AMADIM Fase IV Dr. Gustavo Martínez

Este documento describe las cuatro fases de los estudios clínicos de medicamentos. La Fase I evalúa la seguridad en humanos. La Fase II demuestra la eficacia. La Fase III verifica la seguridad y eficacia a corto y largo plazo. La Fase IV ocurre después de la aprobación para comercialización y recaba datos de seguridad a largo plazo. También describe diferentes diseños de estudios como unicéntricos, multicéntricos, paralelos y cruzados.
Biodisponibilidad y Bioequivalencia de Medicamentos

El documento trata sobre conceptos de biodisponibilidad y bioequivalencia. Explica que la biodisponibilidad evalúa el rendimiento de una forma farmacéutica y que la bioequivalencia compara la biodisponibilidad entre dos productos. También describe los diseños de estudios de bioequivalencia y señala que no todos los productos requieren este tipo de estudios. Por último, resume cómo la ANMAT ha enfocado el tema de la bioequivalencia en Argentina.
Procedimientos Básicos en Medicina - HEMORRAGIAS

En el presente Power Point se explica el tema de hemorragias en el curso de Procedimiento Básicos en Medicina. Se verán las causas, las cuales son por traumatismos, trastornos plaquetarios, de vasos sanguíneos y de coagulación. Asimismo, su clasificación, esta se divide por su naturaleza (externa o interna), por su procedencia (capilar, venosa o arterial) y según su gravedad. Además, se explica el manejo. Este puede ser por presión directa, elevación del miembro, presión de la arteria o torniquete. Finalmente, los tipos de hemorragias externas y en que partes del cuerpo se dan.
Más contenido relacionado
Similar a 15. BIODISPONIBILIDAD Y BIOEQUIVALENCIA_PARTE 3.pdf
Módulo 2 - Farmacovigilancia

Módulo 2 - FarmacovigilanciaCIPPS - Facultad de Medicina de la Universidad Nacional Autónoma de México
El documento trata sobre epidemiología, farmacovigilancia y farmacoepidemiología. En 3 oraciones resume que la epidemiología estudia la distribución y determinantes de la salud y enfermedades en poblaciones humanas, la farmacovigilancia recopila y monitorea información sobre efectos adversos de medicamentos para prevenir daño a pacientes, y la farmacoepidemiología aplica métodos epidemiológicos para integrar información sobre el uso y efectos de fármacos en condiciones reales de práctica clínica.001 Investigacion clinica en farmacologia

El documento proporciona una introducción a los estudios de investigación en farmacología clínica. Explica que estos estudios sistemáticos se realizan en humanos para descubrir los efectos y reacciones de los ingredientes farmacéuticos activos. Detalla las cuatro fases de los estudios clínicos para el desarrollo de nuevos medicamentos, así como los criterios para la participación de voluntarios y el proceso de aprobación regulatoria. En resumen, brinda una visión general del propósito y metodología de los estudios de
Ensayo clinico

Este documento describe los diferentes tipos de estudios clínicos, incluyendo ensayos clínicos. Explica que los ensayos clínicos son estudios experimentales prospectivos que evalúan la eficacia de intervenciones médicas mediante la manipulación intencional de variables y la asignación aleatoria de participantes a grupos. También describe las diferentes fases de los ensayos clínicos y los elementos clave como la aleatorización, enmascaramiento y análisis de datos.
Clinical trials

Este documento proporciona una introducción a los ensayos clínicos. Explica que los ensayos clínicos implican la aplicación de un tratamiento experimental a personas para observar sus efectos. Describe los diferentes tipos de diseños de ensayos clínicos como paralelos y cruzados. También cubre temas como la aleatorización, enmascaramiento, análisis de datos, monitoreo de seguridad, representatividad y generalización de resultados. El objetivo final es evaluar la seguridad y eficacia de nuevos tratam
Farmaepidyvigil

Este documento define la farmacoepidemiología como el estudio de la distribución de los determinantes de la salud y las enfermedades en las poblaciones humanas con respecto al uso y efectos de los fármacos. Describe diferentes tipos de estudios de farmacoepidemiología como estudios de consumo cualitativos y cuantitativos, y estudios de oferta de medicamentos como auditorías terapéuticas. También explica conceptos clave de farmacovigilancia como las clasificaciones de las reacciones adversas a medicamentos y los métodos para evaluar la
Procesos de industrialización de fármacos

Este documento describe el proceso de industrialización de fármacos, incluyendo las etapas de investigación y desarrollo, pre-formulación, pre-clínica, formulación, evaluación, registro y uso. Explica cada etapa del proceso de elaboración de medicamentos, desde la investigación de moléculas hasta los ensayos clínicos y la comercialización. También analiza los efectos adversos de los medicamentos y el mercado farmacéutico mundial.
Glosario

Este documento presenta definiciones de varios términos relacionados con la farmacología y la investigación clínica. Algunos de los términos definidos incluyen absorción, aclaramiento, acontecimiento adverso, adyuvante, aleatorización, alternativas terapéuticas, bioequivalencia, bioética, buenas prácticas clínicas, buenas prácticas de fabricación, buenas prácticas de farmacovigilancia, buenas prácticas de laboratorio, calidad de vida y calidad de
Ensayo clinico controlado modificado

Este documento describe los ensayos clínicos controlados y sus elementos clave. Explica los diferentes tipos de diseños de ensayos como los aleatorizados, los de control concurrente y los históricos. También describe los pasos en la selección de participantes, los tipos de estudios controlados como los abiertos, de simple y doble ciego, y los factores que afectan la interpretación de los resultados.
Desarrollo del medicamento

El documento describe las diversas etapas en el desarrollo de un medicamento, incluyendo estudios preclínicos en animales, 4 fases de ensayos clínicos en humanos para probar seguridad y eficacia, y monitoreo posteriores a la aprobación para detectar efectos adversos inesperados.
Metodo medicina cientifica (1)

Este documento describe tres tipos de investigación clínica y sus características. La investigación clínica se puede clasificar en (1) investigación para aumentar el conocimiento sobre la eficacia y seguridad de un producto, (2) investigación sobre las causas o mecanismos de una enfermedad, y (3) investigación para satisfacer las necesidades de tratamiento de pacientes que han agotado otras opciones. El documento también discute diferentes diseños de estudios clínicos como aleatorizados, controlados, ciegos y otros factores a considerar en la investig
Proceso de desarrollo de fármacos

El proceso de desarrollo de fármacos involucra varias etapas complejas que pueden tomar más de una década. Inicialmente, los científicos diseñan el fármaco conceptualmente identificando un objetivo y estrategia. Luego producen pequeñas cantidades para pruebas preclínicas en animales. Finalmente, realizan tres fases de estudios clínicos en humanos para probar seguridad, dosificación y eficacia a escalas crecientes antes de que las agencias regulatorias autoricen su distribución global,
Ensayos clinicos fase i, ii y iii

Los ensayos clínicos de fase III evalúan la eficacia y seguridad de un tratamiento experimental en una amplia muestra de pacientes representativa, comparándolo con otros tratamientos disponibles de manera controlada, aleatorizada y preferiblemente ciega para reproducir las condiciones de uso habituales y determinar el balance beneficio-riesgo.
ENSAYO CLÍNICO EXPO ANDRES.docx

El documento describe diferentes tipos de ensayos clínicos, incluyendo ensayos unicéntricos versus multicéntricos, ensayos controlados versus no controlados, y diferentes técnicas de enmascaramiento como ensayos simples, dobles o triples ciegos. Explica que los ensayos multicéntricos y controlados son más robustos, mientras que los ensayos no controlados y unicéntricos son más susceptibles a sesgos.
Estudios experimentales en epidemiología

Este documento describe los estudios experimentales en epidemiología. Explica que en este tipo de estudios, el investigador manipula la exposición de un grupo para compararlo con otro grupo no expuesto. Luego describe tres tipos de estudios experimentales: ensayos de campo, que estudian factores preventivos en sujetos sanos; ensayos clínicos, que evalúan tratamientos en pacientes; y ensayos comunitarios, que incluyen intervenciones a nivel comunitario. Finalmente, detalla los pasos para la ejecución de estudios experimentales y sus ventaj
Diseño de un estudio aleatorizado con enmascaramiento

Este documento describe los aspectos clave del diseño de un estudio aleatorizado con enmascaramiento. Explica la importancia de la asignación aleatoria y el enmascaramiento para minimizar la influencia de variables de confusión. Luego, se centra en la elección de las condiciones de intervención y testigo, las variables de respuesta, los efectos adversos, y los criterios de selección de participantes. Finalmente, discute la medición de variables basales, la aleatorización, y el enmascaramiento en el estudio.
Ensayo clinicofase12

Este documento describe las distintas fases de los ensayos clínicos, enfocándose en las fases I y II. Explica que la fase I evalúa la seguridad y tolerabilidad de un nuevo fármaco en un pequeño número de voluntarios sanos, así como su farmacocinética y dosis máxima tolerada. La fase II explora preliminarmente la eficacia y relación dosis-respuesta. Ambas fases ayudan a orientar los estudios posteriores antes de probar el fármaco en pacientes.
Desarrollo y regulación de fármacos

El documento describe los métodos de investigación y desarrollo de nuevos fármacos y su regulación. Explica que los nuevos fármacos se originan en investigaciones públicas y luego son desarrollados por la industria farmacéutica a un alto costo. Detalla las etapas de descubrimiento de fármacos, evaluación preclínica en animales, ensayos clínicos en humanos y aprobación regulatoria considerando factores como seguridad, eficacia y factores de confusión. Finalmente, aborda los retos en el
Taller de iniciación a la investigación clínica. Parte I

Este documento describe diferentes tipos de estudios clínicos, incluyendo estudios descriptivos transversales y longitudinales, estudios analíticos observacionales como estudios de cohortes y casos y controles, y ensayos clínicos. Explica conceptos clave como la clasificación, finalidad, secuenciación temporal, control de asignación a factores de estudio, e inicio del estudio en relación a la cronología de los hechos. Resalta la importancia de considerar factores como la ética, población de estudio, aleatorización, intervención,
AMADIM Fase IV Dr. Gustavo Martínez

Este documento describe las cuatro fases de los estudios clínicos de medicamentos. La Fase I evalúa la seguridad en humanos. La Fase II demuestra la eficacia. La Fase III verifica la seguridad y eficacia a corto y largo plazo. La Fase IV ocurre después de la aprobación para comercialización y recaba datos de seguridad a largo plazo. También describe diferentes diseños de estudios como unicéntricos, multicéntricos, paralelos y cruzados.
Biodisponibilidad y Bioequivalencia de Medicamentos

El documento trata sobre conceptos de biodisponibilidad y bioequivalencia. Explica que la biodisponibilidad evalúa el rendimiento de una forma farmacéutica y que la bioequivalencia compara la biodisponibilidad entre dos productos. También describe los diseños de estudios de bioequivalencia y señala que no todos los productos requieren este tipo de estudios. Por último, resume cómo la ANMAT ha enfocado el tema de la bioequivalencia en Argentina.
Similar a 15. BIODISPONIBILIDAD Y BIOEQUIVALENCIA_PARTE 3.pdf (20)
Diseño de un estudio aleatorizado con enmascaramiento

Diseño de un estudio aleatorizado con enmascaramiento
Taller de iniciación a la investigación clínica. Parte I

Taller de iniciación a la investigación clínica. Parte I
Biodisponibilidad y Bioequivalencia de Medicamentos

Biodisponibilidad y Bioequivalencia de Medicamentos
Último
Procedimientos Básicos en Medicina - HEMORRAGIAS

En el presente Power Point se explica el tema de hemorragias en el curso de Procedimiento Básicos en Medicina. Se verán las causas, las cuales son por traumatismos, trastornos plaquetarios, de vasos sanguíneos y de coagulación. Asimismo, su clasificación, esta se divide por su naturaleza (externa o interna), por su procedencia (capilar, venosa o arterial) y según su gravedad. Además, se explica el manejo. Este puede ser por presión directa, elevación del miembro, presión de la arteria o torniquete. Finalmente, los tipos de hemorragias externas y en que partes del cuerpo se dan.
ATENCIÓN DE PRIMEROS AUXILIOS EN INTOXICACIONES Y ENVENENAMIENTO.pptx

ATENCIÓN DE PRIMEROS AUXILIOS EN INTOXICACIONES Y ENVENENAMIENTO.pptx
FARMACOLOGIA CLASIFICACION DE QUINOLONAS Y FLUOROQUINOLONAS

CLASIFICACION DE QUINOLONAS Y FLUOROQUINOLONAS, TIPOS MEDICAMENTOS, Y GENERACIONES POR MEDICAMENTOS
Valoración nutricional del paciente oncológico

Sesión realizada por una EIR de Pediatría sobre aspectos clave de la valoración nutricional del paciente pediátrico en Oncología, y con tres mensajes para llevarse a casa:
- La evaluación del riesgo y la planificación del soporte nutricional deben formar parte de la planificación terapéutica global del paciente oncológico desde el principio.
- Existe suficiente evidencia científica de que una intervención nutricional adecuada es capaz de prevenir las complicaciones de la malnutrición, mejorar la calidad de vida como la tolerancia y respuesta al tratamiento y acortar la estancia hospitalaria.
- En los hospitales hay pocos dietistas que trabajen exclusivamente en la unidad de Oncología Pediátrica, y esto puede repercutir en mayores gastos sanitarios, peor estado general de los pacientes y menor supervivencia.
MANUAL DE SEGURIDAD PACIENTE MSP ECUADORptx

EN ESTA PRESENTACIÓN SE TRATAN LOS PUNTOS MAS RELEVANTES DEL MANUAL DE SGURIDAD DEL PACIENTE APLICADO EN TODAS LAS INSTITUCIONES DE SALUD PUBLICA DE ECUADOR.
INFECCIONES RESPIRATORIAS AGUDAS EN NIÑOS DEL PERU.pdf

Aqui vemos conceptos relacionados a las infecciones respiratorias.
EL CÁNCER, ¿QUÉ ES?, TIPOS, ESTADÍSTICAS, CONCLUSIONES

El cáncer es una enfermedad caracterizada por el crecimiento descontrolado de células anormales en el cuerpo. Puede afectar a cualquier parte del organismo y su tratamiento varía según el tipo y la etapa de la enfermedad. Los factores de riesgo incluyen la genética, el estilo de vida y la exposición a ciertos agentes carcinógenos. Aunque el cáncer sigue siendo una de las principales causas de morbilidad y mortalidad en el mundo, los avances en la detección temprana y el tratamiento han mejorado las tasas de supervivencia. La investigación continúa en busca de nuevas terapias y métodos de prevención. La concienciación sobre el cáncer es fundamental para promover estilos de vida saludables y fomentar la detección precoz.
Patologia de la oftalmologia (parpados).ppt

Presentación con información a la especialidad de la oftalmología.
Se encontrara información con respecto a las enfermedades encontradas cerca a los ojos (los parpados).
herencia multifactorial, genetica clinica

La predisposición genética no garantiza que una persona desarrollará una enfermedad específica, sino que aumenta el riesgo en comparación con individuos que no tienen esa predisposición genética.
Último (20)
ATENCIÓN DE PRIMEROS AUXILIOS EN INTOXICACIONES Y ENVENENAMIENTO.pptx

ATENCIÓN DE PRIMEROS AUXILIOS EN INTOXICACIONES Y ENVENENAMIENTO.pptx
FARMACOLOGIA CLASIFICACION DE QUINOLONAS Y FLUOROQUINOLONAS

FARMACOLOGIA CLASIFICACION DE QUINOLONAS Y FLUOROQUINOLONAS
Mensuraciones y ponderaciones en la atención primaria

Mensuraciones y ponderaciones en la atención primaria
INFECCIONES RESPIRATORIAS AGUDAS EN NIÑOS DEL PERU.pdf

INFECCIONES RESPIRATORIAS AGUDAS EN NIÑOS DEL PERU.pdf
EL CÁNCER, ¿QUÉ ES?, TIPOS, ESTADÍSTICAS, CONCLUSIONES

EL CÁNCER, ¿QUÉ ES?, TIPOS, ESTADÍSTICAS, CONCLUSIONES
Lavado social, higiénico o médico y quirúrgico de las manos.pdf

Lavado social, higiénico o médico y quirúrgico de las manos.pdf
15. BIODISPONIBILIDAD Y BIOEQUIVALENCIA_PARTE 3.pdf
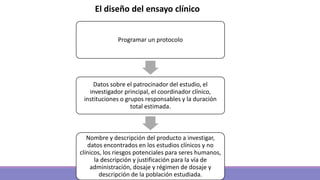
- 1. El diseño del ensayo clínico Programar un protocolo Datos sobre el patrocinador del estudio, el investigador principal, el coordinador clínico, instituciones o grupos responsables y la duración total estimada. Nombre y descripción del producto a investigar, datos encontrados en los estudios clínicos y no clínicos, los riesgos potenciales para seres humanos, la descripción y justificación para la vía de administración, dosaje y régimen de dosaje y descripción de la población estudiada.
- 3. Condición de administración de medicamentos Obtención y manipulación de las muestras biológicas -Por lo general la administración se realiza en ayunas -Verificar la ingesta de líquidos Con los tiempos de toma de muestra se decide tras una prueba piloto, en la que los tiempos seleccionados permitan delimitar todas las fases que configuran las curvas de niveles plasmáticos y éstos deberán seguirse hasta que haya pasado de 3 a 5 tiempos de vida
- 4. Número de voluntarios Criterios de inclusión y exclusión Es necesario conocer la variabilidad (coeficiente de variación) de los valores de AUC, esto basándose en un estudio piloto, de ensayo clínicos previos o datos publicados. Los voluntarios que sean sensibles a los fármacos de estudio deberán ser excluidos de igual manera a mujeres embarazadas o sujetos con enfermedades importantes porque no se los puede tener con tratamiento mientras se realiza el ensayo Los sujetos deben ser de ambos sexos, con una edad de 18 a 55 años de edad y peso que esté dentro del rango del 10-15% del peso ideal para su altura y sexo
- 6. •AUC, Cmax y Tmax Criterios de bioequivalencia Evaluación de enantiómeros
- 7. La seguridad y tolerancia Para la valoración de la tolerancia de un fármaco, se registran y describen temporalmente todos los efectos adversos comunicados espontáneamente por los voluntarios. Se recomienda que al inicio de cada visita y coincidiendo con la administración del fármaco y con cada una de las extracciones de sangre se pregunte sobre la posible aparición de efectos adversos. Valorar la causalidad de un evento adverso La valoración de la intensidad de la reacción adversa se hace también según una escala arbitraria, definida previamente de tres grados (leve, moderada, grave).
- 8. Consideraciones éticas Naturaleza y propósito del estudio Procedimientos a ser realizados Responsabilidades del voluntario como gozar de buena salud y no estar en tratamiento médico en el momento del estudio, acudir a las internaciones en las fechas y horarios informados Posibles riesgos y disconformidades como consecuencia de la administración de los fármacos Beneficios y compensaciones Indemnización, que deberá ser de acuerdo al tiempo dedicado en la realización del citado estudio clínico
- 9. ¿Por qué se pueden obtener diferencias en los ensayos de las formulaciones? 1. La secuencia u orden de administración de las formulaciones (efecto secuencia) 2. El período de administración (efecto período) 3. La formulación que se ha administrado (efecto formulación) 4. El posible efecto del fármaco administrado en el primer periodo sobre el fármaco administrado en el segundo período (efecto carry-over) 5. El diferente comportamiento del fármaco en los individuos (variabilidad interindividual) 6. Otros factores externos (variabilidad intraindividual)
- 11. ENSAYO IN VITRO: Estudio de disolución La disolución es una práctica que consiste en dispersar una sustancia en el seno de un líquido hasta nivel molecular o iónico. Los estudios de disolución se utilizan como herramientas para garantizar la calidad del producto, la uniformidad de diferentes lotes de producción, para determinar la bioequivalencia entre medicamentos genéricos y como guía para el desarrollo de nuevas formulaciones durante el proceso de fabricación Es una prueba que estima la liberación del principio activo a partir de la forma dosificada, evalúa la variabilidad interlote en cuanto a características de liberación y predice la biodisponibilidad y bioequivalencia de productos fabricados.
- 12. Pruebas de disolución La prueba consiste en determinar la cantidad de principio activo que se disuelve, luego de evaluarse un mínimo de 12 dosificaciones a disolución. Se debe determinar los perfiles de disolución en puntos múltiples de 2, 5, 10, 15, 20, 25, 30 minutos a diferentes velocidades de agitación, tipos de medios de disolución y temperaturas. Toma de muestra Comparar con el estándar
- 13. Velocidad de disolución Cantidad de fármaco que se disuelve en una unidad de tiempo a partir a partir de la forma farmacéutica sólida. 50, 75 y 100 rpm Controlada por un disolutor