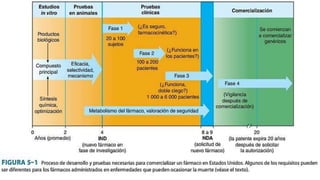
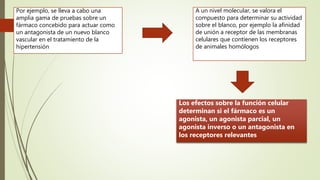
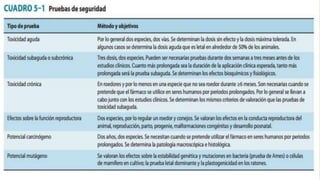
El documento describe los métodos de investigación y desarrollo de nuevos fármacos y su regulación. Explica que los nuevos fármacos se originan en investigaciones públicas y luego son desarrollados por la industria farmacéutica a un alto costo. Detalla las etapas de descubrimiento de fármacos, evaluación preclínica en animales, ensayos clínicos en humanos y aprobación regulatoria considerando factores como seguridad, eficacia y factores de confusión. Finalmente, aborda los retos en el