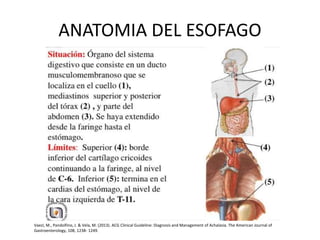
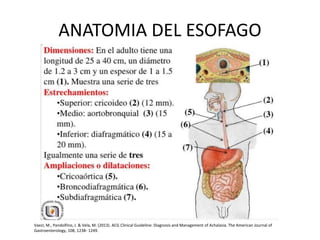
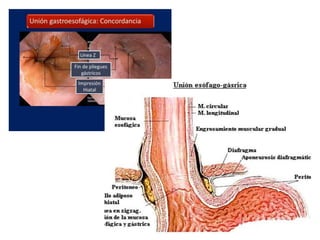
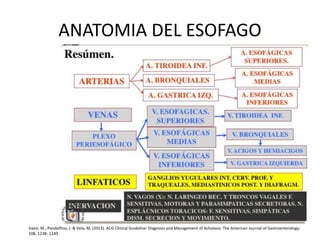
La acalasia es un desorden esofágico caracterizado por la falta de relajación del esfínter esofágico inferior y la pérdida de la peristalsis, presentándose clínicamente con síntomas como disfagia y regurgitación de alimentos. El diagnóstico se realiza a través de endoscopía y manometría, mientras que el tratamiento puede incluir terapia médica, endoscópica o quirúrgica, siendo la dilatación endoscópica y la miotomía de Heller las opciones más efectivas. La acalasia tiene una prevalencia de entre 10 a 12 casos por cada 100,000 personas, afectando más a mujeres y presentándose comúnmente entre los 25 y 60 años de edad.