1. El documento describe diferentes tipos de alcoholes y fenoles, incluyendo sus nombres, propiedades y usos.
2. Los alcoholes primarios, secundarios y terciarios se diferencian por el número de sustituyentes alquílicos unidos al átomo de carbono con el grupo hidroxilo.
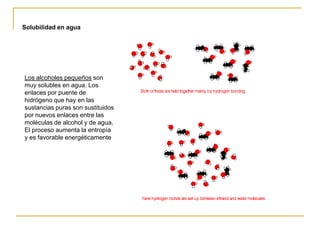
3. Los alcoholes más pequeños como el metanol y el etanol son muy solubles en agua debido a los puentes de hidrógeno, mientras que la solubilidad disminuye con alcoholes más grandes.