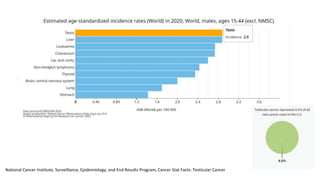
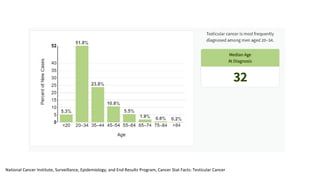
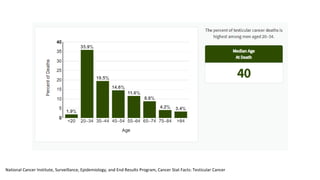
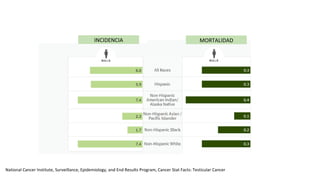
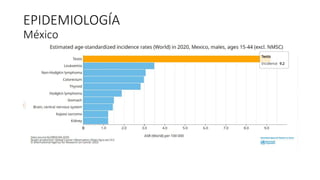
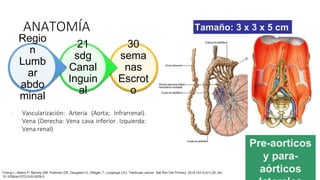
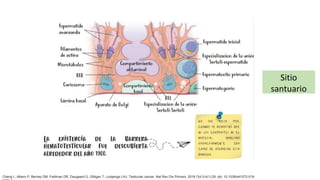
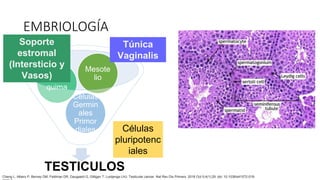
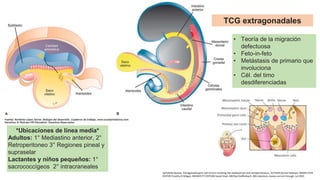
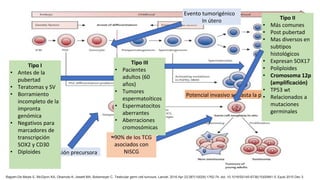
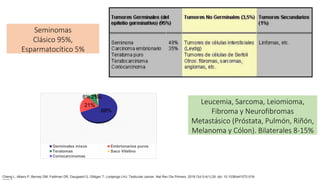
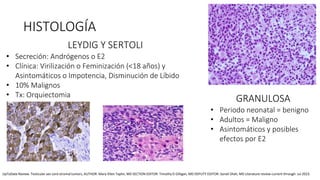
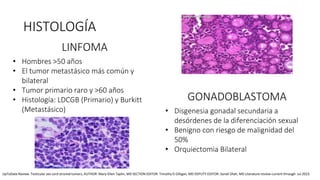
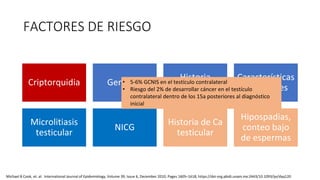
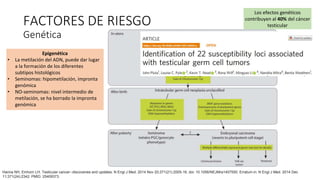
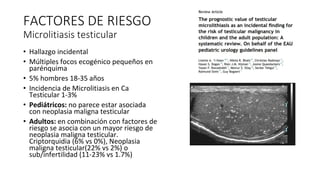
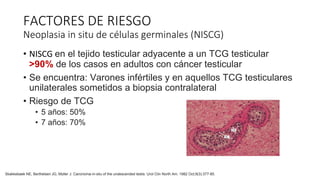
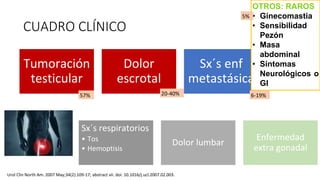
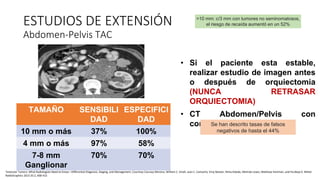
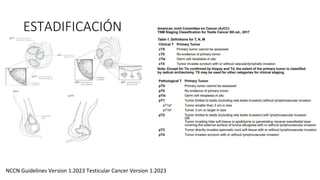
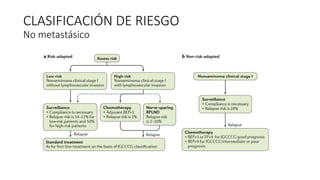
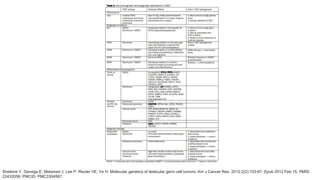
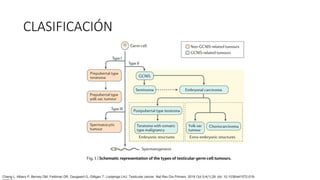
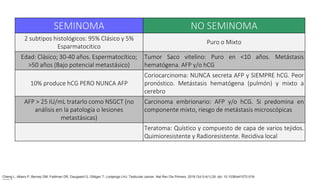
Este documento proporciona información general sobre el cáncer testicular, incluyendo su epidemiología, anatomía, factores de riesgo, cuadro clínico, diagnóstico y clasificación. El cáncer testicular es el más común en hombres de 15-44 años y su incidencia ha aumentado en las últimas décadas. Los factores de riesgo incluyen criptorquidia, historia familiar, características perinatales y neoplasia in situ de células germinales. El cuadro clínico puede incluir una masa