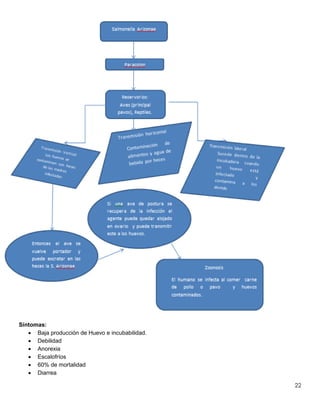
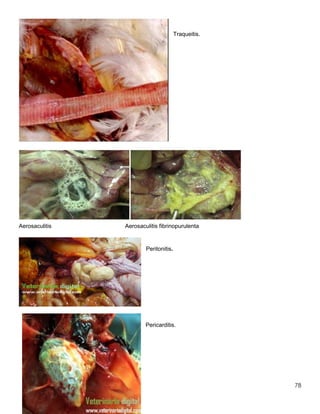
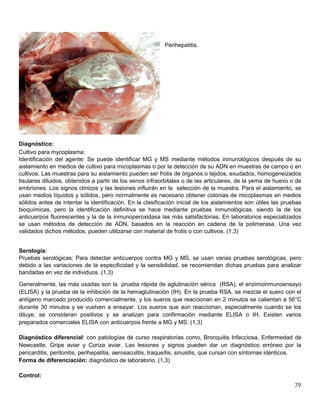
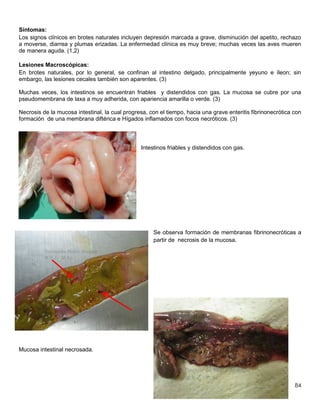
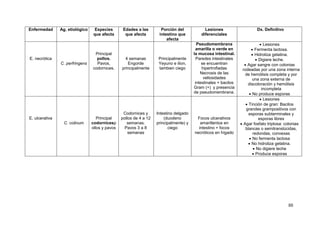
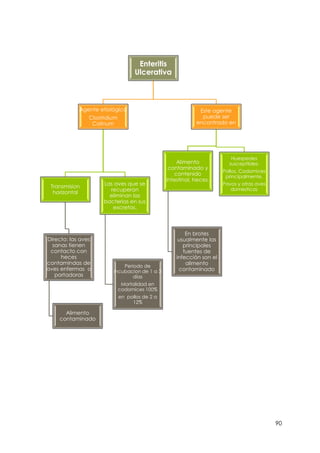
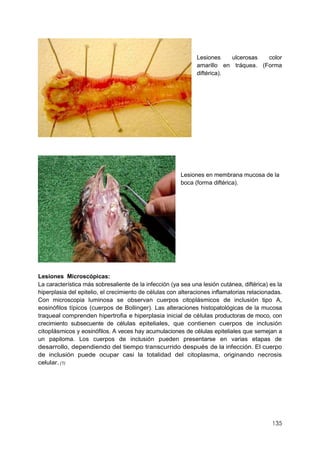
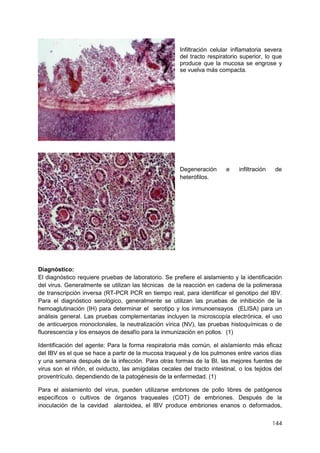
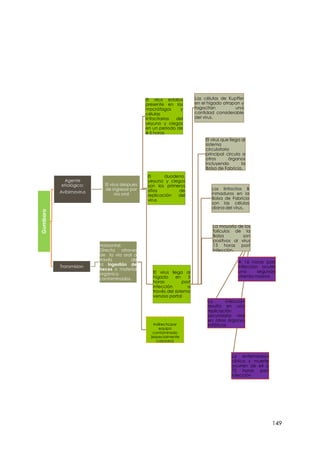
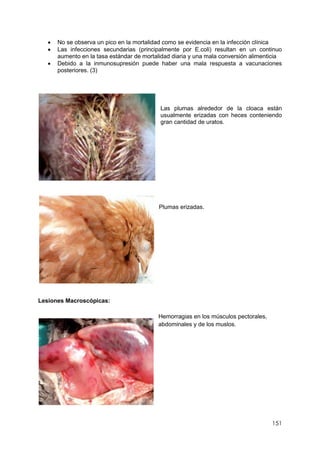
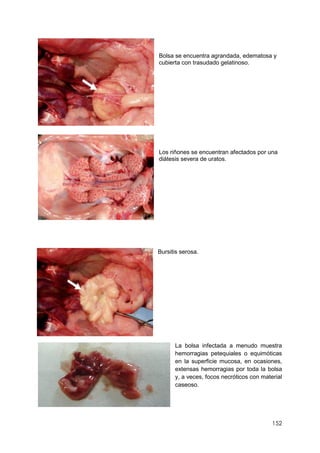
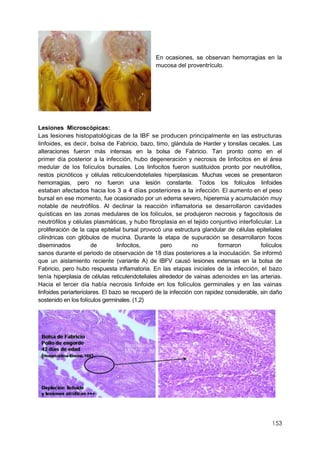
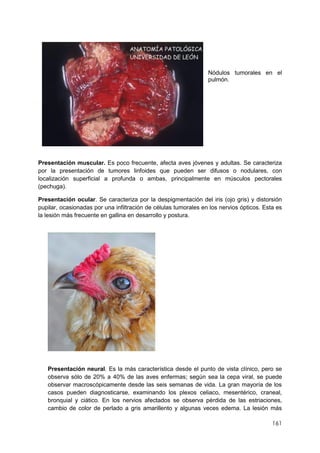
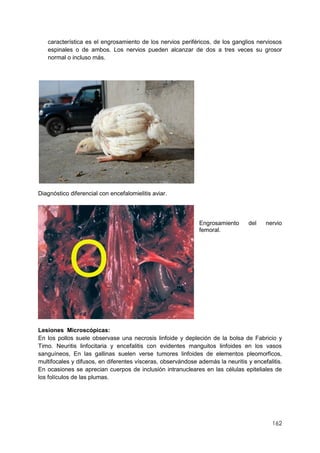
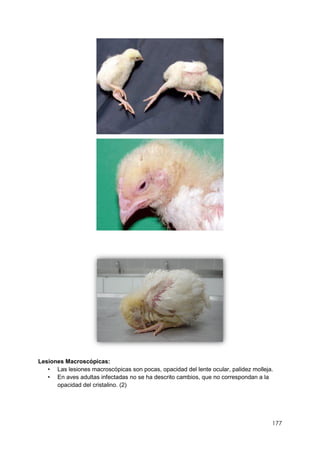
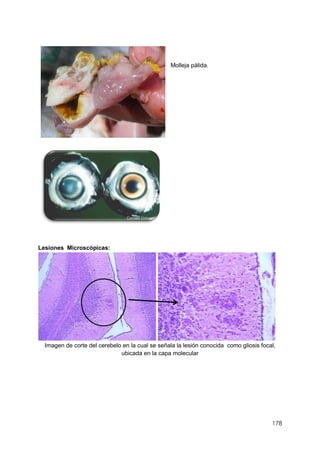
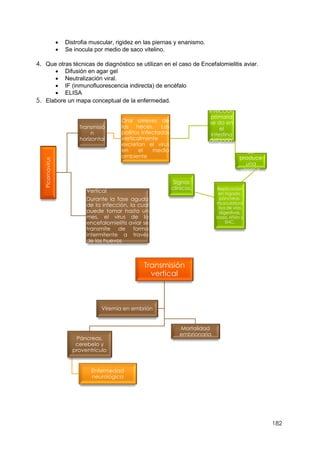
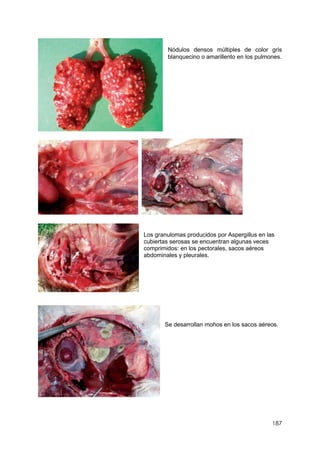
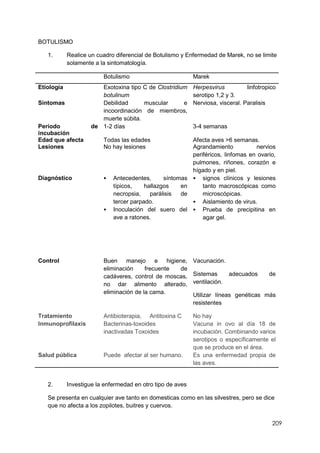
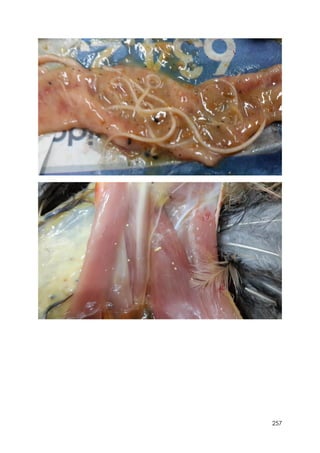
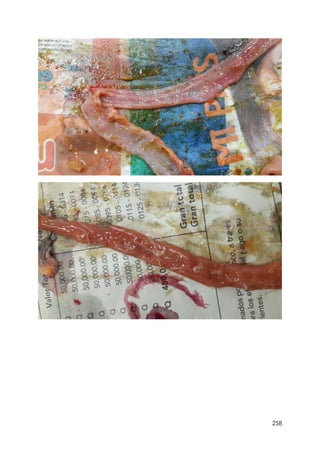
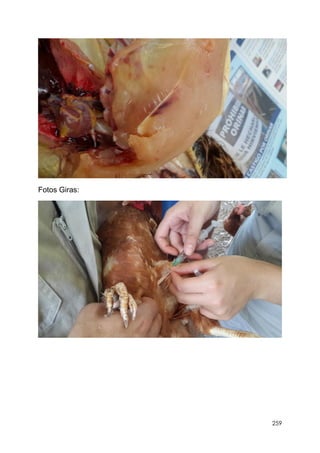
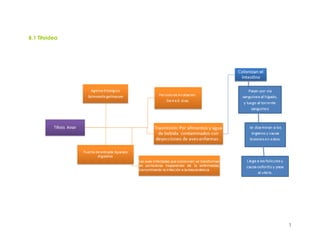
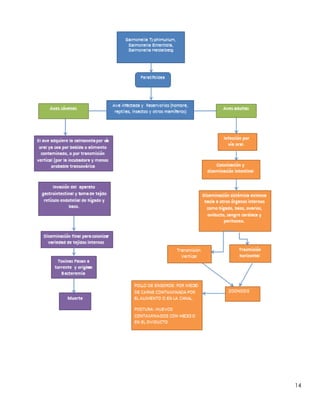
Este documento resume información sobre la enfermedad paratifoidea aviar. La enfermedad es causada por diferentes serotipos de Salmonella que afectan a las aves y pueden causar diarrea, deshidratación y alta mortalidad. Los síntomas incluyen plumas erizadas, heces en las alas, ceguera y cojera. Las lesiones comunes son hepatomegalia, esplenomegalia y enteritis necrótica. El diagnóstico definitivo requiere el aislamiento e identificación de la bacteria Salmonella a partir





















![20
a) Producción de substancias antimicrobianas (bacteriocinas y ácidos grasos volátiles [AGV] que suprimen las
poblaciones o especies patógenas).
b) Estímulo inmune de células residentes, especialmente de células presentadoras de antígenos.
c) Exclusión competitiva, asociada a la competencia por lugares de adhesión en la mucosa.
d) Competencia de nutrientes.
e) Protección de las vellosidades y superficies absorbentes contra toxinas irritantes producidas por
microrganismos patógenos, permitiendo la regeneración de la mucosa lesionada.
Han sido utilizados diferentes microrganismos, varias espécies de Lactobacillus, Saccharomyces cerevisiae,
Aspergillus oryzae, Enterococcus faecium, Bifidobacterium bifidum y otras.
Inmunoprofiláxis: La vacunación es una herramienta eficaz en la prevención de las infecciones por
Salmonella, las vacunas disponibles contra la salmonelosis pueden ser divididas en tres grandes grupos:
vacunas inactivadas conteniendo bacterias completas, vacunas sub-unidades y vacunas vivas atenuadas, las
cuales son utilizadas actualmente en aves. La eficacia de las preparaciones de vacunas es evaluada
generalmente por el nivel de colonización intestinal y sistémica así como la morbilidad y mortalidad después
de la vacunación. (1,3)
Sin embargo, el nivel de protección de un biológico depende de otros factores, entre los cuales se pueden
mencionar: la cepa de desafío, la vía de administración, la dosis infectante, la edad o línea de aves utilizada,
entre otras. En consecuencia, es difícil comparar la eficacia de las vacunas que actualmente están disponibles
para la prevención o el control de la salmonelosis en aves. (1,3)
La vacunación en aves como método de prevención y control de Salmonella, está dirigido básicamente a tres
aspectos: a) Prevenir o reducir la colonización intestinal; b) Prevenir la infección sistémica y; c) Reducir la
excreción fecal. Previniendo la infección sistémica se reduce la colonización en el tracto reproductivo y por lo
tanto se previene la transmisión vertical del microrganismo, y reduciendo la colonización intestinal y excreción
fecal se reduce la contaminación de la carcasa, huevo y el medio ambiente (cama), relacionada
principalmente a la transmisión horizontal de la bacteria. (1,3)
La vacunación es considerada como un costo adicional en la industria avícola. La decisión de establecer
programas de vacunación debe estar de acuerdo con la gravedad del problema en la región o área, y con los
programas establecidos por las industrias o por los servicios oficiales, después de un estudio epidemiológico
serio. (1,3)
Cuestionario:
1. ¿Qué agentes causan la Salmonellas Paratifoideas?
Salmonella enteritidis PT 4, Salmonella typhimurium, Salmonella Heidelberg.
2. ¿Cómo se da la zoonosis? Carne contaminada por el alimento o la canal. Huevos contaminados con
heces en el oviducto.
3. ¿En qué edad se presenta la sintomatología típica de la enfermedad?
Sobre todo en pollitos recién nacidos o aves jóvenes ya que son más susceptibles ante este agente,
mientras que las adultas ya presentan un grado de resistencia y pueden ser asintomáticas.
4. ¿Por qué la salmonella puede causar muerte en aves jóvenes?](https://image.slidesharecdn.com/carpetaornitopatologia-160104212320/85/Carpeta-ornitopatologia-26-320.jpg)