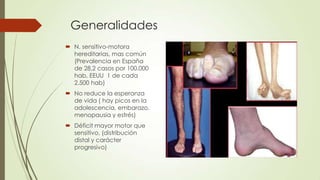
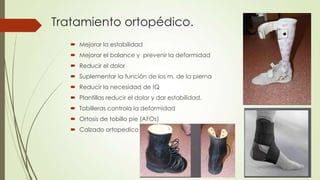
Este caso clínico describe a un paciente de 34 años con una historia familiar de trastornos de la marcha y síntomas de debilidad y dolor en las piernas que sugieren una neuropatía sensitivomotora hereditaria periférica. Los exámenes electrofisiológicos y el estudio genético confirmaron el diagnóstico de enfermedad de Charcot-Marie-Tooth, una enfermedad hereditaria de las neuronas motoras y sensoriales periféricas. El tratamiento se centró en la rehabilitación, el soporte ortop