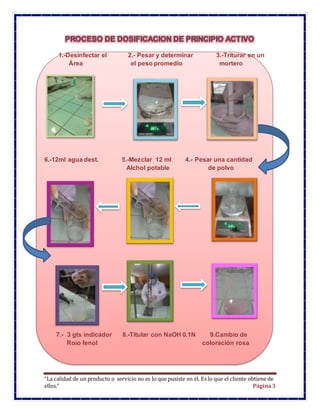
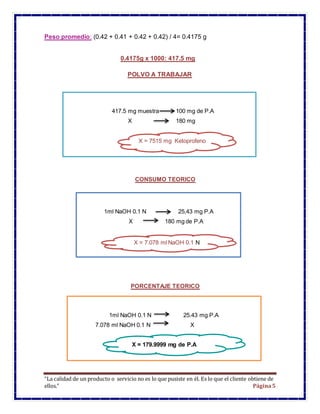
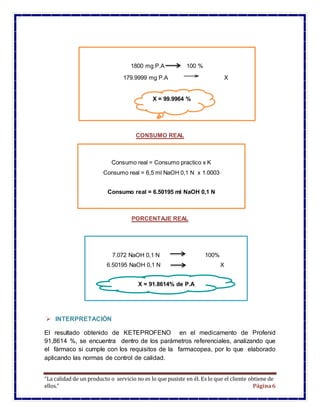
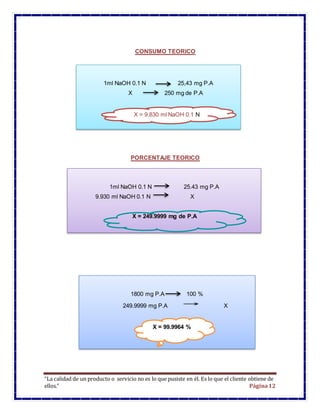
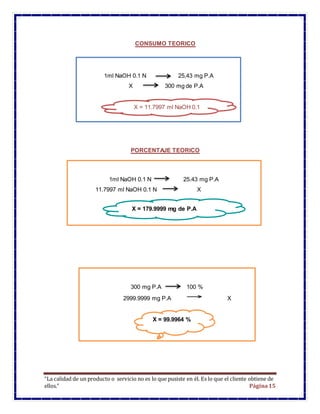
Este documento presenta los resultados de un estudio de control de calidad de un medicamento llamado Profenid que contiene ketoprofeno. Se realizó un análisis titrimétrico para determinar el porcentaje de principio activo y se encontró que contenía un 91,86% de ketoprofeno, lo cual está dentro de los parámetros aceptables. El resumen concluye que el medicamento cumple con los requisitos de calidad.