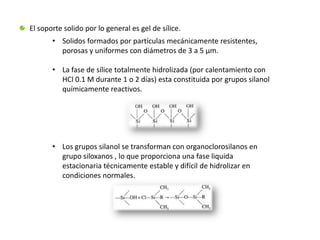
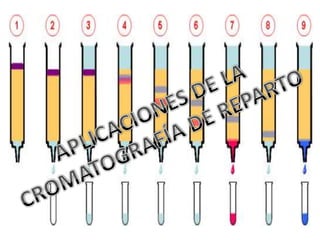
Este documento describe la cromatografía de partición, un método cromatográfico desarrollado en los años 1940. Explica que usa una fase estacionaria líquida anclada a un soporte sólido y una fase móvil líquida inmiscible. También describe los tipos de columnas usadas, incluyendo columnas de fase líquida unida, y explica cómo la polaridad de la fase estacionaria y móvil afecta la elución de los compuestos.