Ejercicios repaso leyes de los gases
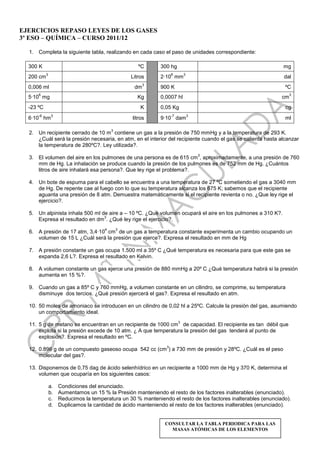
- 1. EJERCICIOS REPASO LEYES DE LOS GASES 3º ESO – QUÍMICA – CURSO 2011/12 1. Completa la siguiente tabla, realizando en cada caso el paso de unidades correspondiente: 300 K ºC 300 hg mg 3 8 3 200 cm Litros 2·10 mm dal 3 0,006 ml dm 900 K ºC 6 3 5·10 mg Kg 0,0007 hl cm -23 ºC K 0,05 Kg cg -6 3 -7 3 6·10 hm litros 9·10 dam ml 3 2. Un recipiente cerrado de 10 m contiene un gas a la presión de 750 mmHg y a la temperatura de 293 K. ¿Cuál será la presión necesaria, en atm, en el interior del recipiente cuando el gas se calienta hasta alcanzar la temperatura de 280ºC?. Ley utilizada?. 3 3. El volumen del aire en los pulmones de una persona es de 615 cm , aproximadamente, a una presión de 760 mm de Hg. La inhalación se produce cuando la presión de los pulmones es de 752 mm de Hg. ¿Cuántos litros de aire inhalará esa persona?. Que ley rige el problema?. 4. Un bote de espuma para el cabello se encuentra a una temperatura de 27 ºC sometiendo el gas a 3040 mm de Hg. De repente cae al fuego con lo que su temperatura alcanza los 675 K; sabemos que el recipiente aguanta una presión de 8 atm. Demuestra matemáticamente si el recipiente revienta o no. ¿Que ley rige el ejercicio?. 5. Un alpinista inhala 500 ml de aire a – 10 ºC. ¿Qué volumen ocupará el aire en los pulmones a 310 K?. 3 Expresa el resultado en dm . ¿Qué ley rige el ejercicio?. 4 3 6. A presión de 17 atm, 3,4·10 cm de un gas a temperatura constante experimenta un cambio ocupando un volumen de 15 L ¿Cuál será la presión que ejerce?. Expresa el resultado en mm de Hg 7. A presión constante un gas ocupa 1.500 ml a 35º C ¿Qué temperatura es necesaria para que este gas se expanda 2,6 L?. Expresa el resultado en Kelvin. 8. A volumen constante un gas ejerce una presión de 880 mmHg a 20º C ¿Qué temperatura habrá si la presión aumenta en 15 %?. 9. Cuando un gas a 85º C y 760 mmHg, a volumen constante en un cilindro, se comprime, su temperatura disminuye dos tercios. ¿Qué presión ejercerá el gas?. Expresa el resultado en atm. 10. 50 moles de amoniaco se introducen en un cilindro de 0,02 hl a 25ºC. Calcule la presión del gas, asumiendo un comportamiento ideal. 3 11. 5 g de metano se encuentran en un recipiente de 1000 cm de capacidad. El recipiente es tan débil que explota si la presión excede de 10 atm. ¿ A que temperatura la presión del gas tenderá al punto de explosión?. Expresa el resultado en ºC. 3 12. 0.896 g de un compuesto gaseoso ocupa 542 cc (cm ) a 730 mm de presión y 28ºC. ¿Cuál es el peso molecular del gas?. 13. Disponemos de 0,75 dag de ácido selenhídrico en un recipiente a 1000 mm de Hg y 370 K, determina el volumen que ocuparía en los siguientes casos: a. Condiciones del enunciado. b. Aumentamos un 15 % la Presión manteniendo el resto de los factores inalterables (enunciado). c. Reducimos la temperatura un 30 % manteniendo el resto de los factores inalterables (enunciado). d. Duplicamos la cantidad de ácido manteniendo el resto de los factores inalterables (enunciado). CONSULTAR LA TABLA PERIODICA PARA LAS MASAS ATÓMICAS DE LOS ELEMENTOS