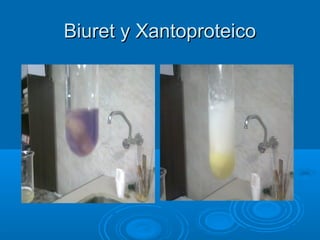
El documento resume una práctica de laboratorio sobre proteínas. En la primera parte, se realizaron ensayos de xantoproteico y biuret para identificar la presencia de proteínas en diferentes sustancias. En la segunda parte, se estudió la diálisis colocando una solución con sales y proteínas en un dializador sumergido en agua. Las pruebas posteriores mostraron que las sales habían pasado a través de la membrana del dializador al agua circundante, mientras que las proteínas permanecieron dentro del dializ