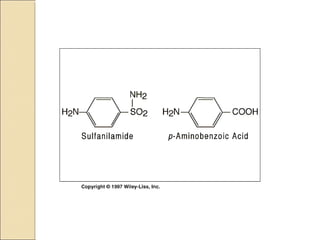
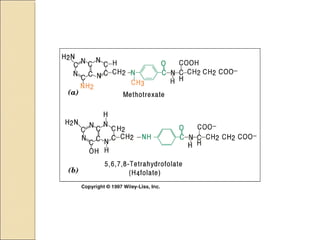
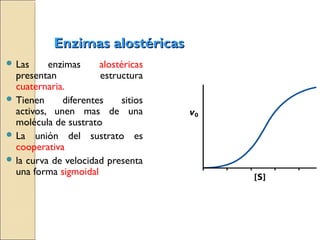
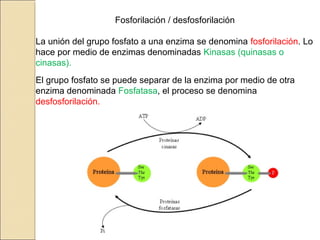
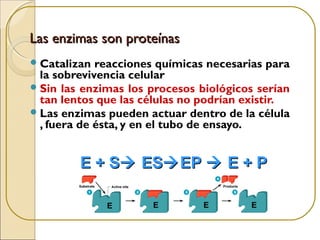
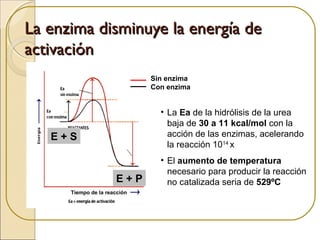
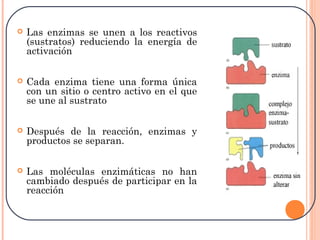
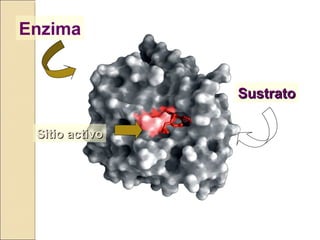
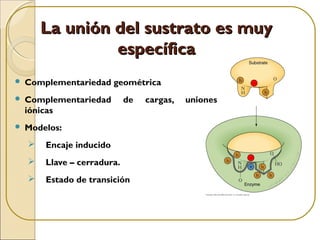
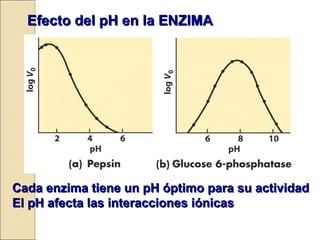
Las enzimas son proteínas que catalizan reacciones químicas necesarias para la vida celular. Cada enzima tiene un sitio activo que reduce la energía de activación de las reacciones, acelerándolas enormemente. Las enzimas aumentan la velocidad de las reacciones bioquímicas actuando como catalizadores específicos y regulables.











![v
[s]
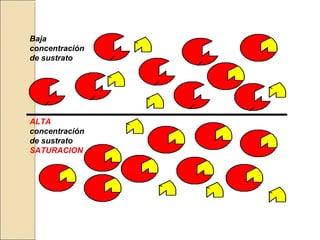
Efecto de la concentración de substrato
.
.
.
. . . . .](https://image.slidesharecdn.com/enzimas1-130907134354-/85/Enzimas-1-19-320.jpg)
![dt
t
s
p
[ ]
Concepto de velocidad inicial
d[P]
v = , t 0](https://image.slidesharecdn.com/enzimas1-130907134354-/85/Enzimas-1-20-320.jpg)

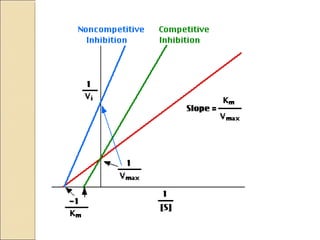
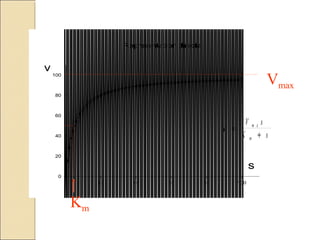
![Relación entre Km yVmaxRelación entre Km yVmax
Michaelis y MentenMichaelis y Menten
Concentración de Sustrato [S]
Velocidaddelareacción(v)
Km
Vmax
Vmax/2
La Km es la concentración de sustrato
donde se obtiene la mitad de la Vmax](https://image.slidesharecdn.com/enzimas1-130907134354-/85/Enzimas-1-22-320.jpg)
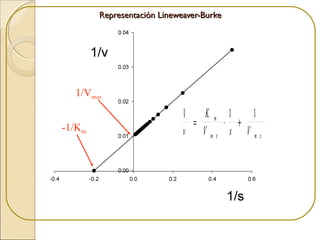
![Concentración de Sustrato [S]
Velocidaddelareacción(v)
Km
Vmax
Vmax/2
A mayor Km, menor es la afinidad de la enzima por el sustrato
A menor Km mayor es la afinidad de la enzima por el sustrato](https://image.slidesharecdn.com/enzimas1-130907134354-/85/Enzimas-1-23-320.jpg)
















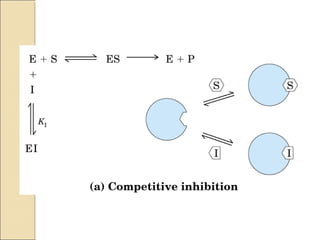
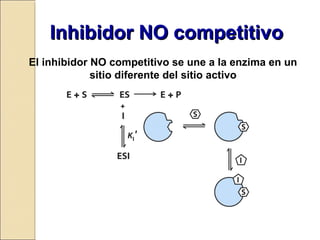
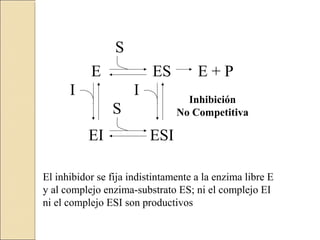
![E ES
EI
I
S
E + P
Características:
- Las fijaciones de substrato e inhibidor son mutuamente excluyentes
- A muy altas concentraciones de substrato desaparece la inhibición
- Por lo general, el inhibidor competitivo es un análogo químico del
substrato.
- El inhibidor es tan específico como el substrato
Se define una constante de
equilibrio de disociación del
inhibidor:
Ki =
[E] [I]
[EI]](https://image.slidesharecdn.com/enzimas1-130907134354-/85/Enzimas-1-44-320.jpg)