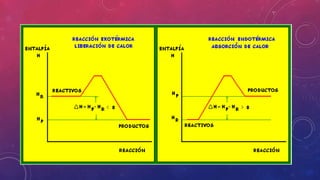
El documento trata sobre conceptos fundamentales de equilibrio químico. Explica que el equilibrio químico ocurre cuando las concentraciones de reactivos y productos se estabilizan, formándose y deshaciéndose a la misma velocidad. También define la constante de equilibrio como la relación entre las concentraciones de reactivos y productos en equilibrio. Finalmente, detalla algunos factores que afectan la velocidad de las reacciones químicas, como la temperatura, estado de los reactivos y su concentración.



![Constante de equilibrio
En el equilibrio las concentraciones de reactivos y productos
permanecen constantes en determinadas condiciones de
presión y temperatura. A la relación que hay entre estas
concentraciones, expresadas en molaridad [mol/L], se le llama
constante de equilibrio.
El valor de la constante de equilibrio depende de la
temperatura del sistema, por lo que siempre tiene que
especificarse.](https://image.slidesharecdn.com/equilibrioqumico-141125163407-conversion-gate01/85/Equilibrio-qu-imico-4-320.jpg)







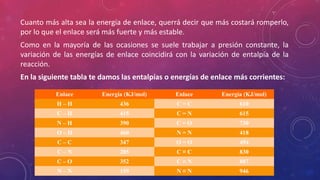












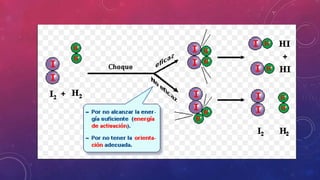
![Concentración de los reactivos
Si los reactivos están en disolución o son gases encerrados en un recipiente,
cuanto mayor sea su concentración, más alta será la velocidad de la reacción en
la que participen, ya que, al haber más partículas en el mismo espacio,
aumentará el número de colisiones.
El ataque que los ácidos realizan sobre algunos metales con desprendimiento de
hidrógeno es un buen ejemplo, ya que este ataque es mucho más violento
cuanto mayor es la concentración del ácido.
Para una reacción: aA + bB ® cC + dD
La variación de la velocidad de reacción con los reactivos se expresa, de manera
general, en la forma:
v = k [A]α [B]β](https://image.slidesharecdn.com/equilibrioqumico-141125163407-conversion-gate01/85/Equilibrio-qu-imico-29-320.jpg)







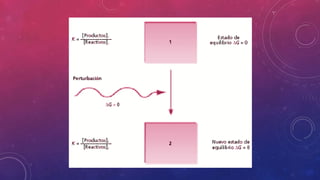

![Adición o eliminación de un reactivo o producto
Consideremos el siguiente equilibrio químico:
CO(g) + Cl2(g) Û COCl2(g)
para el que, a una cierta temperatura, se tiene:
Si se añade más cloro al sistema, inmediatamente después de la adición tenemos:
[Cl2]>[Cl2]eq1 [CO]=[CO]eq1 [COCl2]=[COCl2]eq1
Entonces:
Por tanto, el sistema no se encuentra en equilibrio. Para restablecer el equilibrio debe aumentar
el numerador y disminuir el denominador. Es decir, el sistema debe de evolucionar hacia la
formación del COCl2 (hacia la derecha).
Si disminuimos las concentraciones de CO, de Cl2 o de ambas, el equilibrio se desplaza hacia la
izquierda, ya que tiene que disminuir el numerador.
Un aumento de la concentración de os reactivos, o una disminución de los productos hace que
la reacción se desplace hacia la derecha. En cambio, una disminución de la concentración de los
reactivos, o un aumento de la concentración de los productos, hacen que la reacción se desplace
hacia la izquierda.](https://image.slidesharecdn.com/equilibrioqumico-141125163407-conversion-gate01/85/Equilibrio-qu-imico-40-320.jpg)



