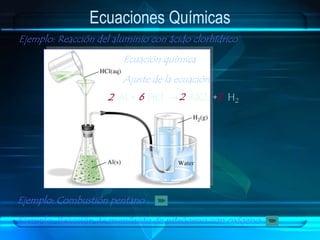
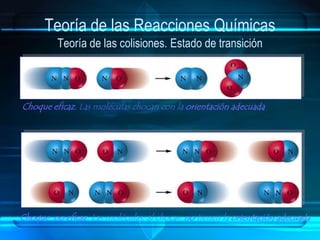
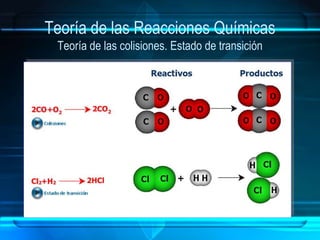
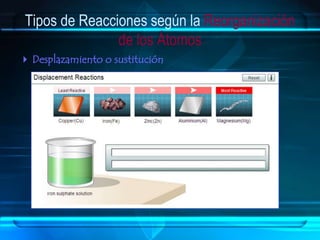
El documento aborda las reacciones químicas, explicando su naturaleza, clasificación y ecuaciones químicas. Detalla el concepto de reactivos y productos, así como factores que influyen en la velocidad de reacción y el intercambio de energía. También se discuten tipos de reacciones y principios como la conservación de la masa en los cambios químicos.