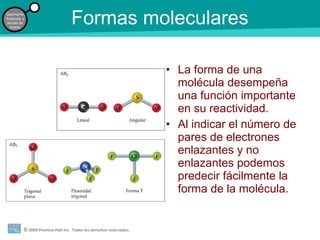
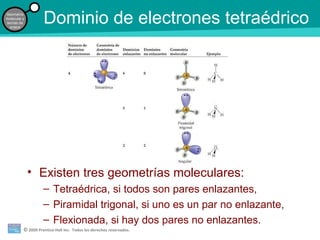
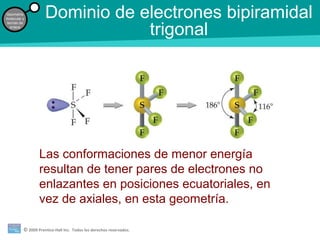
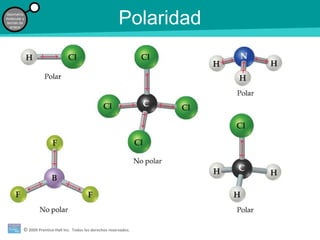
El documento trata sobre la geometría molecular y las teorías de enlace. Explica que la forma de una molécula depende del número de pares de electrones enlazantes y no enlazantes, y que la teoría de repulsión de pares de electrones de la capa de valencia predice la mejor disposición de estos dominios de electrones. También describe los diferentes tipos de hibridación de orbitales atómicos que permiten explicar las geometrías moleculares observadas.