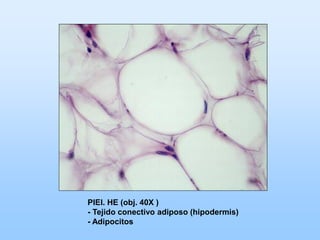
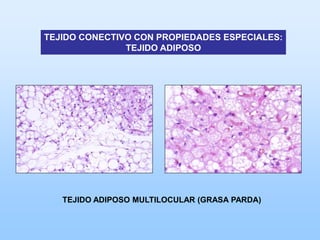
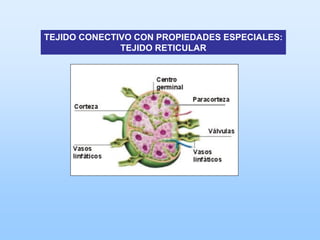
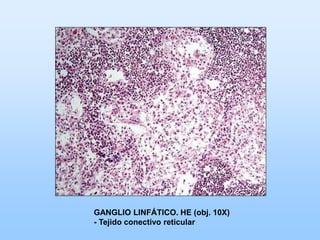
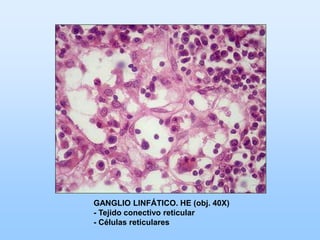
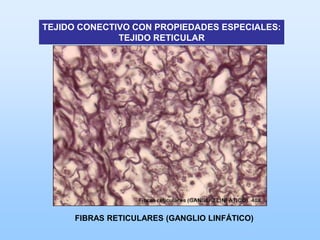
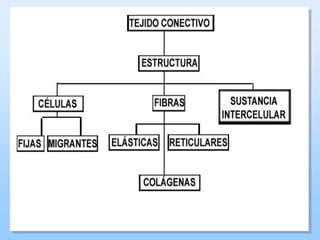
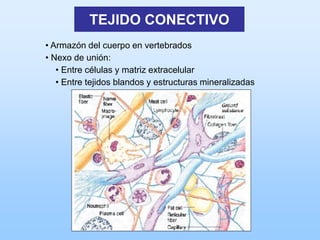
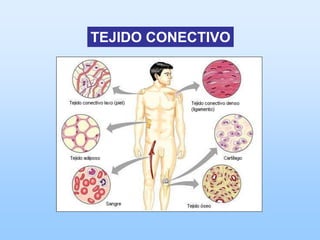
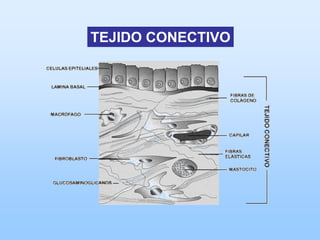
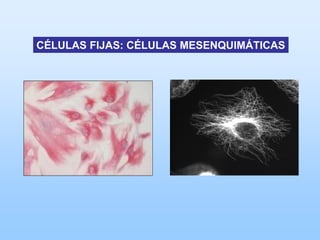
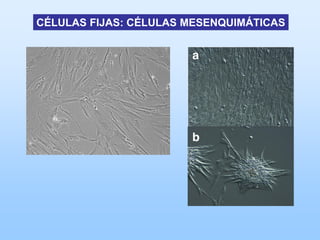
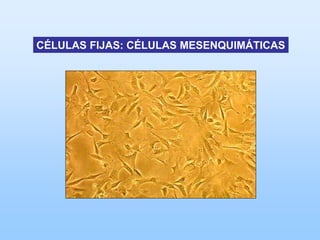
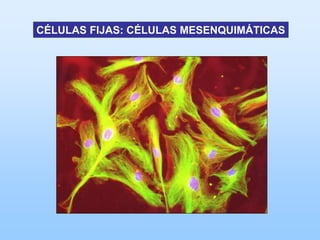
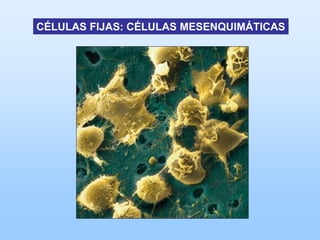
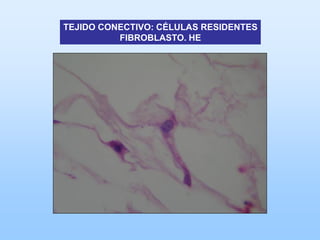
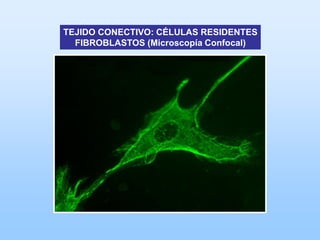
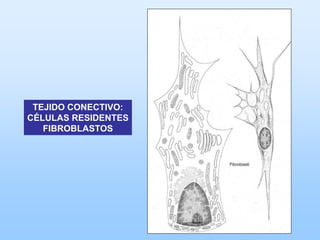
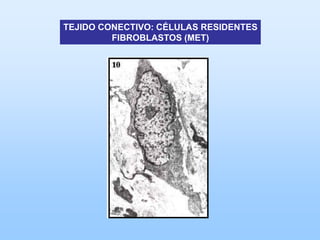
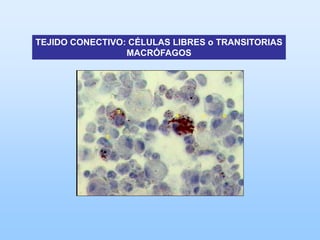
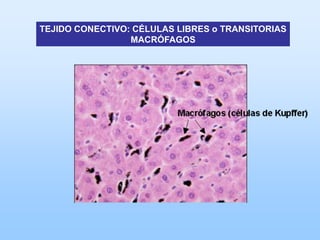
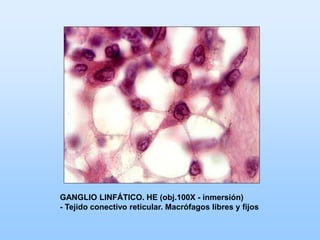
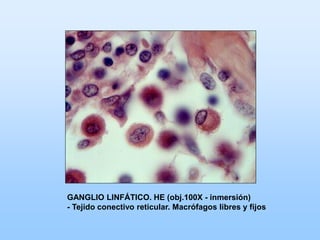
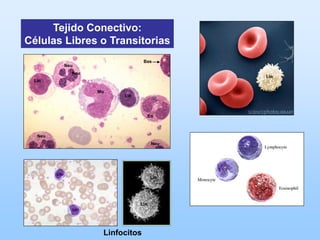
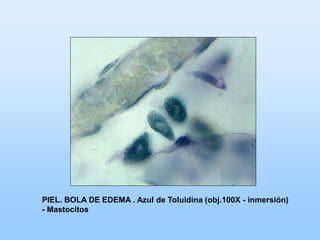
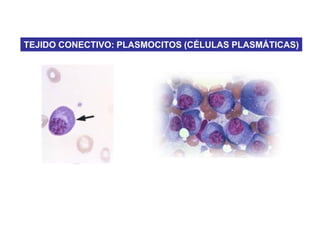
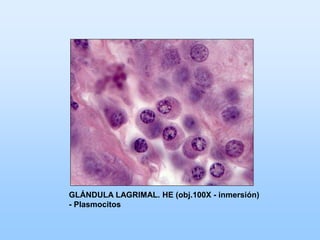
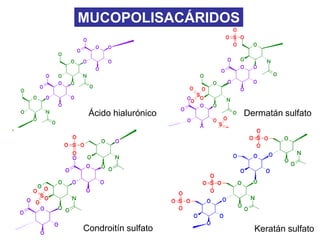
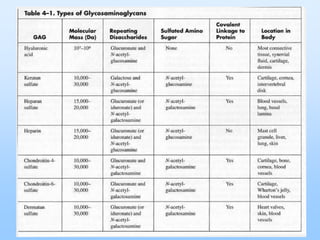
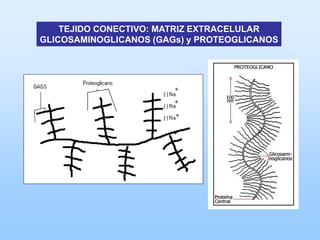
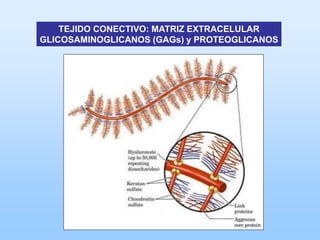
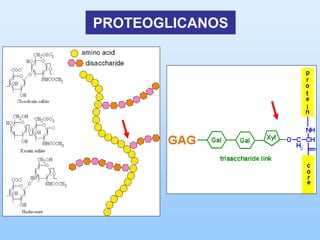
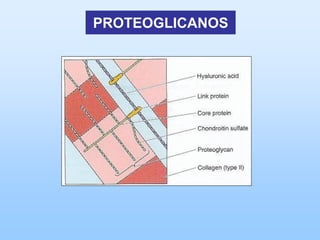
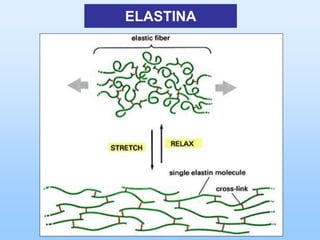
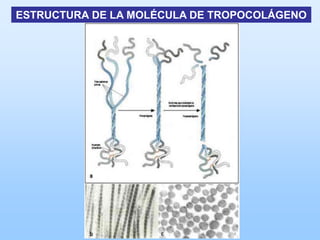
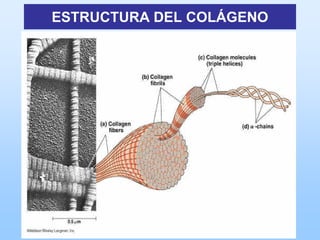
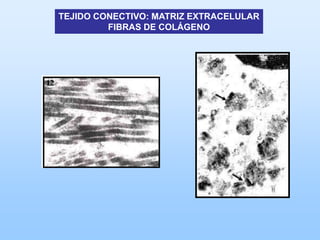
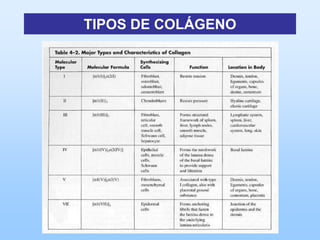
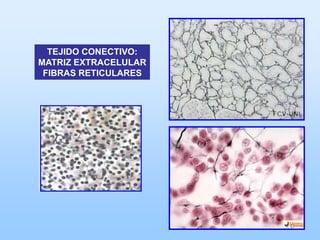
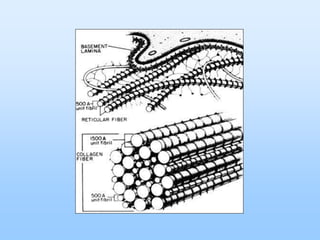
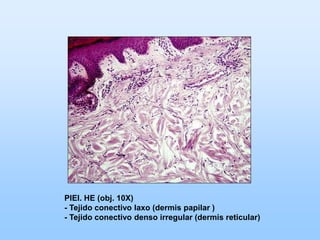
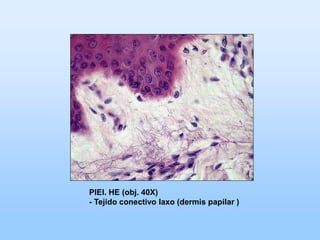
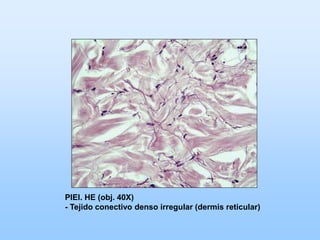
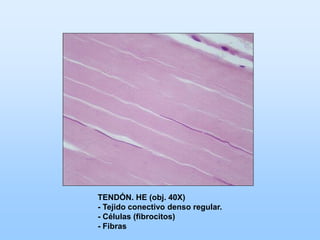
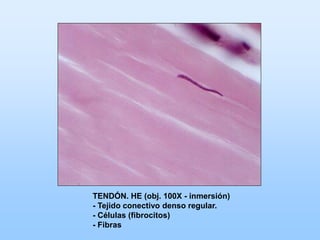
El documento describe las características principales del tejido conectivo, incluyendo sus componentes celulares como fibroblastos y macrófagos, y sus componentes de la matriz extracelular como colágeno, elastina, proteoglicanos y mucopolisacáridos. Explica que el tejido conectivo sirve como soporte y unión entre otros tejidos y estructuras del cuerpo, y que su composición y organización varían según la función de cada tejido.























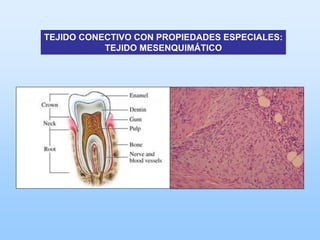
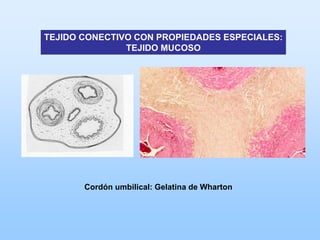
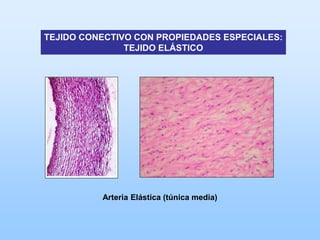
![TEJIDO CONECTIVO CON PROPIEDADES ESPECIALES:
TEJIDO ELÁSTICO
Arteria Elástica [túnica media (b)]](https://image.slidesharecdn.com/histologiatejidoconectivo-121018203658-phpapp01/85/Histologia-tejido-conectivo-82-320.jpg)