Este documento describe un experimento para predecir e interpretar la difusión molecular en estado estacionario a través de películas porosas en líquidos. Se estudió la difusión del hidróxido de potasio en agua a través de dos películas porosas, una de piedra pómez y otra de esponja. El método experimental involucró tomar muestras periódicas para determinar las concentraciones y calcular el flujo difusivo. Los resultados permitieron determinar el perfil de concentraciones y la difusividad efectiva de




![Difusión Molecular en Estado Estacionario en una Película Porosa
OBJETIVOS
1. OBJETIVO GENERAL:
Predecir e interpretar con datos experimentales el Fenómeno de Difusión
Molecular en una película porosa en líquidos para los sistemas Hidróxido de Potasio-
Agua, a través de una Película Porosa (una piedra pómez y la otra en una esponja) en
Estado Estacionario
2. OBJETIVO ESPECÍFICOS:
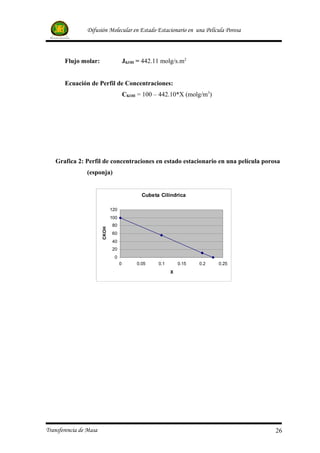
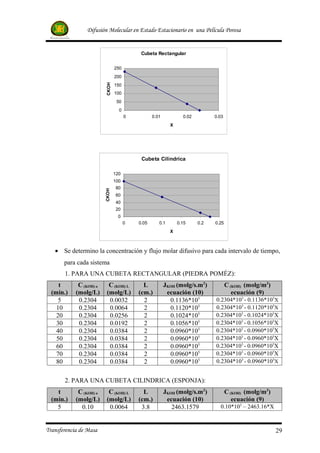
• Determinar el perfil de concentraciones para cada sistema.
• Determinar el flujo molar difusivo para cada sistema.
• Graficar el perfil de concentraciones en estado estacionario para cada sistema.
• Determinar las concentraciones y el flujo molar difusivo del KOH en agua en
intervalos de tiempo para cada sistema.
MARCO TEÓRICO
1. TRANSFERENCIA DE MASA:
• La transferencia de masa, estudia el movimiento de las moléculas entre fase y
fase por medio de mecanismos de difusión, convección y condiciones que les
favorece.
• La transferencia de masa es la transferencia de un constituyente de una región
de alta concentración ajena de baja concentración. [1]
Transferencia de Masa 6](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-5-320.jpg)
![Difusión Molecular en Estado Estacionario en una Película Porosa
1.1 Mecanismos:
En el caso de un fluido en reposo o fluyendo laminarmente en dirección
perpendicular a la gradiente de concentración, la transformación se desarrolla
únicamente como consecuencia del movimiento al azar de las moléculas de la
mezcla. [2]
1.2 Concentración total de masa o densidad:
Es la concentración total de la mezcla contenida en la unidad de volumen. [3]
n
= ∑ i − − − − − − − − − − − − − (1)
i =1
1.3 Fracción de masa (WA):
Es la concentración de la especie A, dividida entre la densidad total de la masa.
[3]
A A
WA = n
= − − − − − − − − − ( 2)
∑
i =1
i
la suma de las fracciones de maza, deben ser uno:
n
∑W i = 1 − − − − − − − − − − − − − −( 3)
i =1
1.4 Concentración molar de la especie A (CA):
Se define como el número de moles de A, presentes por unidad de volumen de
la mezcla. Por definición, un mol de cualquier especie contiene una masa
equivalente a su peso molecular. Los términos de la concentración de masa y de
la concentración molar están relacionados por medio de la siguiente expresión:
[3]
A
CA = − − − − − − − − − − − −( 4 )
MA
1.5 Concentración molar total (C):
Es el número total de moles de la mezcla, contenidos en la unidad de volumen,
esta es: [4]
n
C = ∑ Ci − − − − − − − − − − − −( 5)
i =1
1.6 Fracción molar (XA):
Transferencia de Masa 7](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-6-320.jpg)
![Difusión Molecular en Estado Estacionario en una Película Porosa
La fracción molar correspondiente alas mezclas de líquidos o sólidos, X A, son
las concentraciones molares de la especie A divididas entre la concentración
molar total. [4]
CA
XA = ( líquidos y sólidos ) − − − − − − − − − −( 6)
C
La suma de las fracciones molares debe ser igual a uno, por definición:
n
∑X i = 1 − − − − − − − − − − − − − − − − − − − − − ( 7)
i =1
1.7 Velocidades:
Es un sistema de componentes múltiples, las diferentes especies se moverán de
manera normal a diferentes velocidades. [4]
1.7.1 Velocidad promedio o media de la masa:
Se define en función de las densidades y velocidades de la masa, de todas
las componentes. [3]
n
∑ V i i n
iVi
V = i =1
n
=∑ − − − − − − − − − − − ( 8)
i =1
∑ i =1
i
1.7.2 Velocidad molar media o promedio:
Se define en función de las concentraciones molares de todos los
componentes, por medio de la expresión. [3]
n
∑C V i i n
CiVi
V= i =1
n
=∑ − − − − − − − − − − − ( 9)
i =1 C
∑C
i =1
i
2. LEY DE FICK PARA LA DIFUSIÓN MOLECULAR:
La difusión molecular (o el transporte molecular) puede definirse como la
transferencia (o el movimiento) de moléculas individuales a través de un fluido por
medio de los movimientos individuales y desordenados de las moléculas.
Podemos imaginar a las moléculas desplazándose en líneas rectas y cambiando su
dirección al rebotar con otras moléculas después de chocar con ellas. Puesto que las
Transferencia de Masa 8](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-7-320.jpg)
![Difusión Molecular en Estado Estacionario en una Película Porosa
moléculas se desplazan en trayectorias desordenadas, a la difusión molecular a veces
se le llama también proceso de camino desordenado.
En la Fig.(1). Se muestra esquemáticamente el proceso de difusión molecular. Se
ilustra la trayectoria desordenada que la molécula A puede seguir al difundirse del
punto (1) al (2) a través de las moléculas de B.
Si hay un número mayor de moléculas de A cerca del punto (1) con respecto
al punto (2). Entonces, y puesto que las moléculas se difunden de manera
desordenada en ambas direcciones, habrá más moléculas de A difundiéndose de (1) a
(2) que de (2) a (1). La difusión neta de A va de una región de alta concentración a
una de baja concentración. [2]
Fig. 1 Diagrama esquemático del proceso de difusión molecular
La ecuación general de la ley de Fick puede escribirse como sigue para una mezcla
de A y B.
dX A
J ∗AZ = −C DAB ..............................................................(10)
dZ
Si C es constante entonces, puesto que.
C A = CX A :
Cd A = d (CX A ) = DC A .............................................................(11)
Sustituyendo esta relación en la relación (10) para una concentración total constante.
Transferencia de Masa 9](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-8-320.jpg)
![Difusión Molecular en Estado Estacionario en una Película Porosa
dC A
J ∗AZ = − DAB ..............................................................(12)
dZ
Esta ecuación es la de uso mas común es muchos procesos de difusión molecular.
3. DIFUSIÓN EN SÓLIDOS POROSOS EN LOS QUE AFECTA LA
ESTRUCTURA:
Poros
Concentración
CA0
Sólido
Fig. 2 Poros del medio en el que tiene lugar la difusión
Este tipo de difusión en sólidos no depende de la estructura real del sólido. La
difusión se verifica cuando el fluido o soluto que se difunde se disuelve en el sólido
para formar una solución más o menos homogénea. [5]
3.1. Difusión de líquidos en sólidos porosos:
La difusión de líquidos en sólidos porosos se uso la ley de fick considerando
al sólido como un material de tipo homogéneo y usando una difusividad
experimental DAB. En este trabajo nos interesan los sólidos porosos que
tienen canales o espacios vacíos interconectados en el sólido, los cuales
afectan a la difusión. [2]
En el caso de que los espacios Estén totalmente llenos de agua liquida, la
concentración de sal en agua en el limite 1 es C A1 y en el punto 2 es C A2 . Al
difundirse en el agua por los volúmenes vacíos, la sal toma una trayectoria
sinuosa desconocida que es mayor que (Z2 – Z1) por un factor r, llamado
Transferencia de Masa 10](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-9-320.jpg)
![Difusión Molecular en Estado Estacionario en una Película Porosa
sinuosidad. (En el sólido inerte no hay difusión). Para la difusión de estado
estable de la sal de una solución diluida. [2]
D AB ( C A1 − C A 2 )
NA = E
− − − − − − − − − − − − (13)
T ( Z1 − Z 2 )
Para sólidos de tipo inerte, r puede variar desde 1.5 hasta 5. En muchos casos
resulta conveniente combinar los terminas en una expresión de difusividad
efectiva. [2]
E
D Aef = D AB m 2 / s − − − − − − − − − − − − − −(14 )
t
FIG. 3 Esquema de un sólido poroso típico
4. EJEMPLO DE DIFUSION EN UN MEDIO POROSO:
Si se tienen un recipiente con dos soluciones separadas por un medio poroso que
están perfectamente agitados tal como se muestra en la siguiente figura.
Transferencia de Masa 11](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-10-320.jpg)

![Difusión Molecular en Estado Estacionario en una Película Porosa
soluto A. a través de la solución 2. ambos efectos de resistencia se determinarán
como difusividad efectiva que depende de la superficie real expuesta a la
transferencia de masa. [1]
Balance de materia
dC A
(WA ) Z − (WA ) Z +AZ = ...........(1)
dz
WA = AS J A
Reemp. (1)
(ASJA)Z-(ASJA)Z+AZ = 0
Dividiendo por AS ∆ Z
( AS J A ) Z (A J )
= − S A Z +∆ Z = 0
AS ∆ Z AS ∆ Z
Aplicando límites:
( J ∆ ) Z + ∆ Z − ( J A )Z
lim =0
∆ z→ 0 ∆Z
Derivada
−dJ A
= 0 ……………(2)
dZ
Ley de Fick para hallar el perfil de Concentraciones:
Aplicando la ley de Fick
dCA
J A = −D
dZ
Para un medio poroso
dCA
J A = −Def
dZ
En (2)
− A
dJ −
d d
= −Def CA =0
dZ dz dZ
2
d CA
Def =0
dZ 2
Integrando:
C A = C1Z + C2 ………………(3)
Evaluando las condiciones de frontera:
Para Z = 0 ; CA = CA0
Transferencia de Masa 13](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-12-320.jpg)





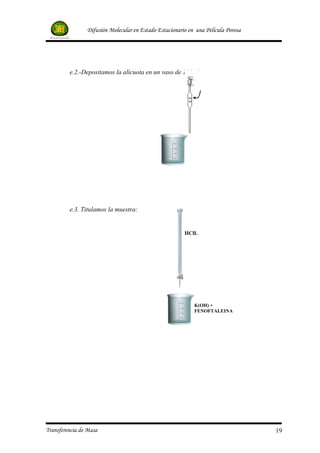






![Difusión Molecular en Estado Estacionario en una Película Porosa
• Asegurar correctamente la película porosa en cada uno de los sistemas.
• Controlar adecuadamente el tiempo con respecto a la toma de datos y hacerlo hasta
que el sistema llegue a ser estacionario, para aplicar las relaciones establecidas.
BIBLIOGRAFÍA
• [1] Teoría del Cuaderno.
Transferencia de Masa 31](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-30-320.jpg)
![Difusión Molecular en Estado Estacionario en una Película Porosa
• [2] CRISTIE J. GEANKOPLIS, “Proceso de Transportes y operaciones Unitarios”,
compañía Editorial Continental S.A., 2 da Edición – México 1995, pag. 320-321-
350.
• [3] JAMES R. WELTY, “Fundamentos de Transferencia de Momento, Calor y
Masa”, Editorial Limusa S.A., Octava reimpresión – México 1997, pag. 533 al 542
• [4] R. B. BIRD, “Fenómenos de Transporte”, Editorial Reverte S.A., Segunda
reimpresión, México, 1995, capitulo 16.
• [5] J. M. SMITH, “Ingeniería de Cinética Química”, Editorial continental S.A.,
1ra. Edición, México, 1992, pag. 301- 305
Transferencia de Masa 32](https://image.slidesharecdn.com/laboratoriodifusinmolecular-121116143418-phpapp02/85/Laboratorio-difusion-molecular-31-320.jpg)