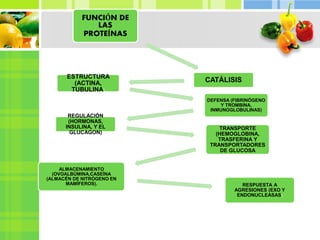
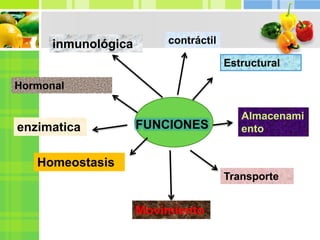
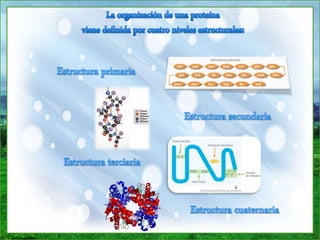
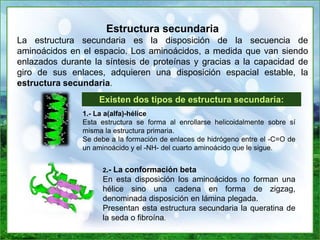
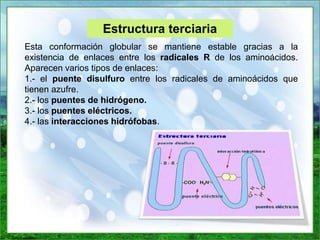
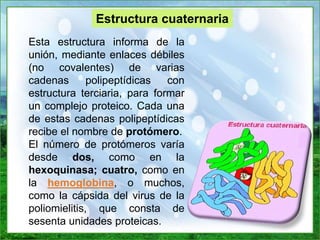
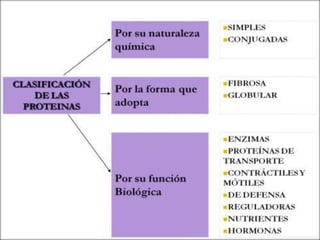
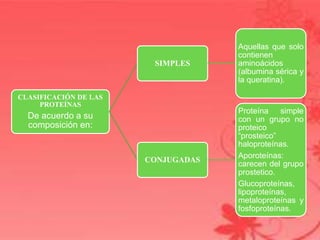
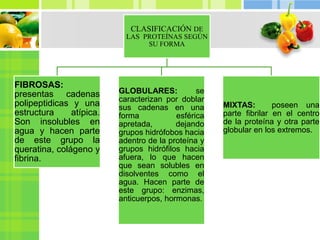
Este documento proporciona información sobre las proteínas. Explica que las proteínas están formadas por cadenas de aminoácidos unidos por enlaces peptídicos y cumplen funciones estructurales, de almacenamiento, transporte, movimiento, homeostasis e inmunológica. Además, describe las diferentes estructuras de las proteínas incluyendo la estructura primaria, secundaria, terciaria y cuaternaria. Finalmente, clasifica las proteínas de acuerdo a su composición en simples y conjugadas, y de ac