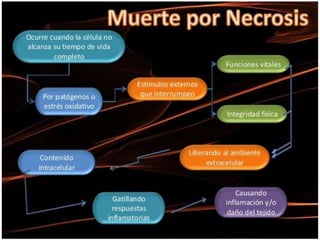
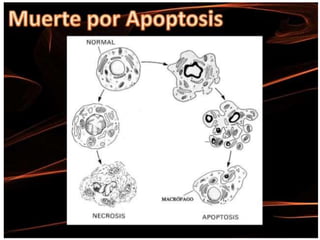
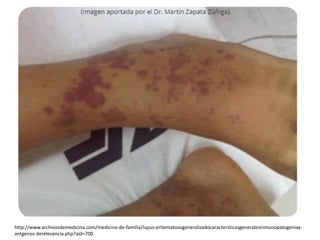
El documento describe la inmunopatogenia del lupus eritematoso sistémico (LES). El LES se caracteriza por la activación e hiperreactividad de los linfocitos B que producen autoanticuerpos dirigidos contra diversos antígenos nucleares y citoplasmáticos. Esto ocurre debido a una deficiencia en la eliminación de restos celulares apoptóticos, lo que expone antígenos modificados y desencadena una respuesta autoinmune. Los principales anticuerpos asociados con el LES incluyen aquellos dir